
(12分)【化学——物质结构与性质】
氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是 。
A.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
B.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
C.基态As原子中,电子占据的最高能级为4d
D.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是 。向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有 和 。
(3)PCl3分子中,Cl-P-Cl键的键角____ 109o28’(填“>”“<”或“=”)。
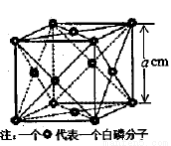
(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。己知该晶体的密度为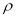 g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。
g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。
(12分)
(1)b(2分)
(2)NH3分子与水分子之间能够形成氢键(2分) 离子键(2分) 配位键(2分)
(3) < (2分)
(4)496/(ρa3) (2分)
【解析】
试题分析:(1)a、以光的形式释放能量时,电子从能量较高的轨道跃迁到能量较低的轨道,错误;b、P为第VA族元素,3p轨道排布3个电子,为半充满状态,更稳定,第一电离能较大,所以P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na,正确;c、基态As原子中,电子占据的最高能级为4p,错误;d、Bi为第六周期第VA族元素,原子中最外层有3个能量相同的电子,错误。
(2)N、O原子半径小而电负性大,NH3分子与水分子之间能够形成氢键,PH3分子与水分子之间不能形成氢键,所以NH3在水中的溶解度比PH3大得多;[Cu(NH3)4]2+与SO42-之间形成了离子键;Cu2+与NH3之间形成了配位键。
(3)PCl3中P原子杂化方式为sp3杂化,分子构型为三角锥型,P原子含有一对孤对电子,对成键电子有较强的排斥作用,所以Cl-P-Cl键的键角<109o28’。
(4)根据晶胞示意图,P4分子位于晶胞的8个顶点和6个面的面心,则1个晶胞含P4分子:8×1/8+6×1/2=4,以1个晶胞为研究对象,ρ=4×124÷NA÷a3,解得NA=496/(ρa3)。
考点:本题考查电子排布、第一电离能、化学键与氢键、分子构型、晶胞的计算。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014山东省潍坊市高三4月模拟考试理综化学试卷(解析版) 题型:简答题
(12分)【化学一有机化学基础】
M是一种重要的粘合剂,其合成路线如下:
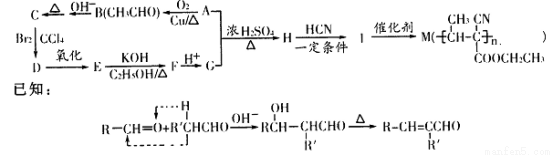
请回答下列问题:
(l)物质C中所含官能团的名称是_________。
(2) H→I的反应类型是_________;检验物质B常用的试剂是_________。
(3) C→D、D→E的反应顺序不能颠倒的原因__________________。
(4)写出与G具有相同的官能团的同分异构体的结构简式:_________。
(5)写出E→F的化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列各组离子在给定条件下能大量共存的是
A.强酸性溶液中:NH4+、K+、ClO-、Cl-
B.有SO42—存在的溶液中:Na+、Mg2+、Ba2+、I-
C.加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br-
D.在含有大量[Al(OH) 4] -的溶液中:NH4+、Na+、Cl-、H+
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——化学与技术】
合成氨工业对国民经济和社会发展具有重要意义,下图是工业合成氨的简要流程示意图。
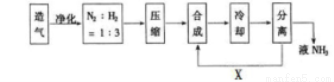
(1)合成氨的原料气往往混有CO2等杂质,在进入合成塔之前需净化,其原因是_______ 。
(2)工业上合成氨选择的适宜条件是:以铁为主的催化剂、_______、________。
(3)沿X路线进入合成塔的物质是_______,这样设计的意义是________。
(4)目前工业制硝酸所采用的主要方法是_______法。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
某有机物的结构如图所示,下列有关它的说法正确的是
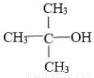
A.能与氢氧化钠溶液反应
B.4个碳原子可能在同一平面内
C.与它具有相同官能团的同分异构体还有4种
D.与乙醇互为同系物
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三二模理综化学试卷(解析版) 题型:选择题
25℃时,向20.00mLNaOH溶液中逐滴加入0.20mo1·L-l的CH3COOH溶液得到如图曲线。下列说法正确的是

A.水电离出的氢离子浓度:a>b
B.c点时恰好中和
C.在d~e之间存在如下关系:C(Na十)>c(CH3COO-)>c(H十)>c(OH一)
D.e点时溶液中溶质是CH3COONa和CH3COOH
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高一下学期期末考试化学试卷(解析版) 题型:实验题
(18分)NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
_____________________________________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A.铁 B.铝 C.铂 D.玻璃
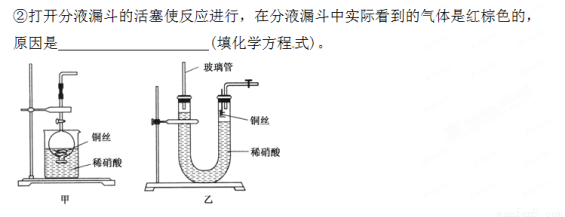
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反就开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是___________________________________。
②让反应停止的操作方法及原因是________________________。
(4)以下收集NO气体的装置,合理的是________(填选项代号)。
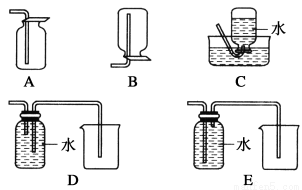
(5)假设实验中12.8 g Cu全部溶解,需要通入标况下________mL O2才能使NO全部溶于水。
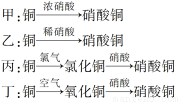
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”),理由是___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高一5月质量检测化学试卷(解析版) 题型:填空题
(11分)A、B、C、D四种短周期元素。原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)写出下列元素的名称:A_______,B ,C_______,D 。
(2)D的质子数和中子数相等,D的原子组成符号为 ,它的最高价为___________价。
(3)用电子式表示A、D两元素形成AD2的过程: ;
写出C2B2的电子式 。
(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是
。
(5)写出甲和A的最高价氧化物反应的化学方式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高二化学试卷(解析版) 题型:选择题
主链含5个碳原子,有甲基、乙基2个支链的烷烃有:( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com