
【题目】同分异构现象是造成有机物种类繁多的重要原因之一。下列互为同分异构体的是
A.甲烷与丙烷B.乙醇与乙酸
C.乙烯与乙烷D.CH3CH2CH2CH3与CH3CH(CH3)2
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】准确量取25.00mL高锰酸钾溶液,可选用的仪器是
A. 25mL酸式滴定管 B. 有刻度的50mL烧杯
C. 25mL碱式滴定管 D. 25mL量筒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A. 水的电离度始终增大 B. c(NH4+)/c(NH3·H2O)先增大再减小
C. c(CH3COOH)+c(CH3COO-)不变 D. 加入氨水的体积为10mL,c(H+)=Kw1/2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气广泛应用于化工、轻工、化肥、制药、合成纤维等领域。
(1)在三个1L的恒容密闭容器中,分別加入0.10molN2和0.30molH2发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。
2NH3(g) △H<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。

①与实验Ⅱ相比,实验Ⅰ、实验Ⅲ分别采用的实验条件为_________、_________。
②实验Ⅲ在0~10 min的平均反应速率v(H2)=_________。
(2)分别以N2、H2为电极反应物,HCl-NH4Cl为电解质溶液制造新型燃料电池,试写出该电池正极的电极反应式:______________________。
(3)常温下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应达平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=_________。
(4)工业上用NH3消除NO、NO2 污染。当n(NO)∶n(NO2) =1∶1时,在高温及催化剂条件下,每生成1mol N2放出热量akJ,请书写该反应的热化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2005年诺贝尔化学奖授予了研究烯烃复分解反应的科学家,以表彰他们作出的卓越贡献。烯烃复分解反应原理如下:C2H5CH=CHCH3 + CH2=CH2 ![]() C2H5CH=CH2 + CH2=CHCH3,现以烯烃C5H10为原料,合成有机物M和N,合成路线如下:
C2H5CH=CH2 + CH2=CHCH3,现以烯烃C5H10为原料,合成有机物M和N,合成路线如下:
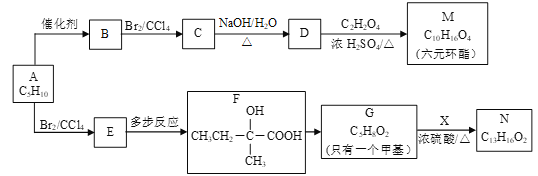
(1)按系统命名法,有机物A的名称是___________。
(2)B的结构简式是___________。
(3)C![]() D的反应类型是___________。
D的反应类型是___________。
(4)写出D![]() M的化学方程式___________。
M的化学方程式___________。
(5)写出E![]() F合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
F合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
(6)已知X的苯环上只有一个取代基,且取代基无甲基,则N的结构简式为___________。
(7)满足下列条件的X的同分异构体共有___________种,写出任意一种的结构简式___________。
①遇FeCl3溶液显紫色 ②苯环上的一氯取代物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是
A. 硫酸亚铁的电离方程式:Fe2(SO4)3 =2Fe3++3SO42-
B. H2SO4的电离方程式:H2SO4=H2+ + SO42-
C. 质子数为6,中子数为7的微粒:76C
D. 钠离子的结构示意图: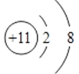
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预言,燃料电池将是21世纪获得电力的重要途径,美国已计划将甲醇燃料电池用于军事目的。一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。回答下列问题:
(1)这种电池放电时发生的化学反应方程式________________。
(2)此电池的正极发生的电极反应式是_______________;负极发生的电极反应式是_________。
(3)电解液中的![]() 离子向__________极移动;向外电路释放电子的电极是__________。
离子向__________极移动;向外电路释放电子的电极是__________。
(4)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化效率高,其次是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为前四周期原子序数依次增大的六种元素,A、C、D原子均有两个未成对电子,A、B、C同周期,A与D、B与F分别同主族,E是生活中用量最大的金属。请回答下列问题:
(1)E比较稳定的离子核外电子排布式_____________________________.
(2)A、B、C的第一电离能由小到大的顺序为_________________![]() 用元素符号表示
用元素符号表示![]() 、B、C的简单氢化物中最易汽化的物质的化学式___________.
、B、C的简单氢化物中最易汽化的物质的化学式___________.
(3)C与D形成的物质的晶体类型是____________,IT产业中该晶体用于生产____________.
(4)由A、B、C三种元素中的一种或两种元素形成的分子中,有的互为等电子体,写出其中一组等电子体的化学式:______![]() 并写出对应的结构式_______________.
并写出对应的结构式_______________.
(5)B的单质晶胞与![]() 的相似,则一个晶胞中含B的原子个数为____
的相似,则一个晶胞中含B的原子个数为____![]() 与氢形成的分子空间构型是_______.
与氢形成的分子空间构型是_______.
(6)“砒霜”是一种含C,F的化合物,其分子结构如图1所示,该化合物的分子式为F4C6,F原子采取______杂化;C,D,E组成的化合物的晶胞如图2,其晶胞参数为a pm,则其密度为___________________g/cm3(列出式子即可,阿伏伽德罗常数为NAmol-1)。
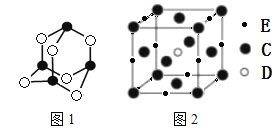
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com