
| m |
| M |
| V |
| Vm |
| m |
| M |
| 20g |
| 20g/mol |
| 11.2L |
| 22.4L/mol |
| 9g |
| 18g/mol |


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
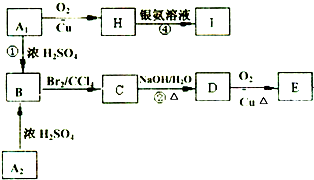 同分异构体A1和A2分别与浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的52倍,含碳的质量分数为92.3%.在催化剂存在下,1mol B可以和4mol H2发生加成反应.核磁共振氢谱显示,H有5个吸收峰.有关物质之间的转化关系如下:
同分异构体A1和A2分别与浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的52倍,含碳的质量分数为92.3%.在催化剂存在下,1mol B可以和4mol H2发生加成反应.核磁共振氢谱显示,H有5个吸收峰.有关物质之间的转化关系如下:查看答案和解析>>
科目:高中化学 来源: 题型:
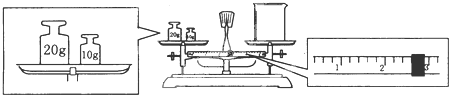
查看答案和解析>>
科目:高中化学 来源: 题型:
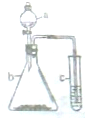 利用如图装置进行实验,仪器a、b、c中分别盛装下列试剂,试管c中现象描述正确的是( )
利用如图装置进行实验,仪器a、b、c中分别盛装下列试剂,试管c中现象描述正确的是( )| 选项 | a | b | c | c试管中现象 |
| A | 浓硫酸 | Na2SO3 | BaCl2溶液 | 产生白色沉淀 |
| B | 稀盐酸 | 大理石 | 苯酚钠溶液 | 产生白色沉淀 |
| C | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液褪色 |
| D | 浓硝酸 | 铜片 | KI淀粉溶液 | 溶液变蓝 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
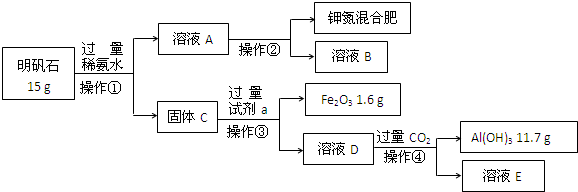
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
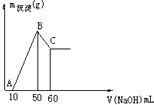
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com