
6.4 g铜与一定量的浓硝酸充分反应后,铜反应完全,硝酸的还原产物有NO、NO2,反应后溶液中所含H+物质的量为n mol,此时溶液中所含NO3-的物质的量为
A.0.28 mol B.0.31 mol C.(n + 0.2) mol D.(n + 0.4) mol
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
非选择题 【共道小题,分】【14分】下图是实验室验证某铜银合金完全溶解于一定量的浓硝酸时,生成NO2气体中含有NO的实验装置。常温下,NO2与N2O4混合存在,在低于0 ℃时,几乎只有白色N2O4晶体存在。
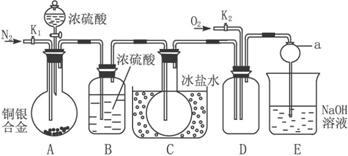
(1)反应前打开A部分的活塞K1,持续通一段时间氮气,其理由是_____________________
_____________________________________________________________________。
(2)若装置中缺B部分,其后果是__________________________________________________。
(3)反应结束后,打开D部分的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热的氧气,则瓶内气体的颜色比前者更深,其原因是__________________________。
(4)E部分中a仪器所起的作用是______________________________________________。
(5)已知该铜银合金的质量为15 g,加入40 mL 135 mol·L-1的浓硝酸,实验结束后,A部分烧瓶内溶液中的c(H+)=1 mol·L-1(假设反应中HNO3既无挥发也无分解,体积仍为40 mL)。
①参加反应硝酸的物质的量为_____________________。
②为测定铜银合金中铜的质量分数,还需要进行的主要实验操作是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
6.4 g铜与一定量的浓硝酸充分反应后,铜反应完全,硝酸的还原产物有NO、NO2,
反应后溶液中所含H+物质的量为n mol,此时溶液中所含NO3-的物质的量为
A.0.28 mol B.0.31 mol C.(n + 0.2) mol D.(n + 0.4) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用![]() 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A.7.8 g ![]() 晶体中阳离子和阴离子的总个数为0.4
晶体中阳离子和阴离子的总个数为0.4![]()
B.标准状况下,1.12![]() 所含的原子总数是0.2
所含的原子总数是0.2![]()
C.![]() 和
和![]() 的混合气体中所含的分子数一定为
的混合气体中所含的分子数一定为![]()
![]()
D.3.2g铜与一定量的浓硝酸完全反应生成的气体分子数是0.1![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
用![]() 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A.7.8 g ![]() 晶体中阳离子和阴离子的总个数为0.4
晶体中阳离子和阴离子的总个数为0.4![]()
B.标准状况下,1.12![]() 所含的原子总数是0.2
所含的原子总数是0.2![]()
C.![]() 和
和![]() 的混合气体中所含的分子数一定为
的混合气体中所含的分子数一定为![]()
![]()
D.3.2g铜与一定量的浓硝酸完全反应生成的气体分子数是0.1![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com