
设nA为阿伏加德罗常数的数值,下列说法正确的是 ( )
A.常温下,4 g CH4含有nA个C—H共价键
B.1 mol Fe与足量的稀HNO3反应,转移2nA个电子
C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1nA个HCO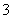
D.常温常压下,22.4 L的NO2和CO2混合气体含有2nA个O原子
答案 A
解析 特别注意反应物的量对Fe与稀HNO3反应产物的影响。A项4 g CH4的物质的量为n(CH4)=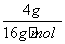 =0.25 mol,1个CH4分子含有4个C—H键,则0.25 mol CH4含有1 mol(即nA个)C—H共价键;B项Fe与足量稀HNO3反应生成Fe(NO3)3,1 mol Fe反应时,转移3 mol(即3nA个)电子;C项n(NaHCO3)=0.1 mol·L-1×1 L=0.1 mol,但HCO
=0.25 mol,1个CH4分子含有4个C—H键,则0.25 mol CH4含有1 mol(即nA个)C—H共价键;B项Fe与足量稀HNO3反应生成Fe(NO3)3,1 mol Fe反应时,转移3 mol(即3nA个)电子;C项n(NaHCO3)=0.1 mol·L-1×1 L=0.1 mol,但HCO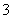 发生水解和微弱电离,则1 L该溶液中含有HCO
发生水解和微弱电离,则1 L该溶液中含有HCO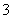 的物质的量小于0.1 mol(即个数少于0.1nA);D项常温常压下,22.4 L的NO2和CO2混合气体的物质的量并非1 mol,含有的O原子也不是2nA个。
的物质的量小于0.1 mol(即个数少于0.1nA);D项常温常压下,22.4 L的NO2和CO2混合气体的物质的量并非1 mol,含有的O原子也不是2nA个。


科目:高中化学 来源: 题型:
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:

(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是__________;滤渣可循环使用,滤渣的主要成分是________(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO)∶n(NO2)>1∶1,则会导致__________________;若n(NO)∶n(NO2)<1∶1,则会导致_________________。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为_______________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图表示各物质之间的转化关系。已知D、E、Z是中学化学常见的单质,其他都是化合物。Z、Y是氯碱 工业的产品。D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂。E为日常生活中应用最广泛的金属。除反应①外,其他反应均在水溶液中进行。请回答下列问题。
工业的产品。D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂。E为日常生活中应用最广泛的金属。除反应①外,其他反应均在水溶液中进行。请回答下列问题。

(1)写出下列物质的化学式:B____________、G_____________________________、Y______________。
(2)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则E是__________极,请写出在此电极上发生的电极反应式:
________________________________________________________________________。
(3)写出反应①的化学方程式______________________________________________。
(4)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp=2.097×10-39。将
0.01 mol·L-1的A溶液与0.001 mol·L-1的NaOH溶液等体积混合,你认为能否形成沉淀________(填“能”或“不能”),请通过计算说明___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由阿伏加德罗常数(NA)和一个水分子的质量(m水)、一个水分子的体积(V水)不能确定的物理量是________。
①1摩尔水的质量 ②1摩尔水蒸气的质量 ③1摩尔水蒸气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
N0为阿伏加德罗常数的值。下列叙述正确的是 ( )
A.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0
B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0
C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0
查看答案和解析>>
科目:高中化学 来源: 题型:
将a g二氧化锰粉末加入c L b mol·L-1的浓盐酸中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.可以收集到氯气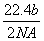 L
L
B.反应后溶液中的Cl-数目为
C.NA可表示为
D.反应后溶液中的H+数目为bc-2d
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计如图所示的装置分别进行不同的探究实验(夹持装置已略去),请回答下列问题:

| 实验 | 药品 | 制取气体 | 量气管中液体 |
| Ⅰ | Cu、稀HNO3 | NO | H2O |
| Ⅱ | NaOH(s)、浓氨水 | NH3 | |
| Ⅲ | 电石、饱和NaCl溶液 | C2H2 | H2O |
| Ⅳ | 镁铝合金、NaOH溶液 | H2 | H2O |
(1)如何检验如图所示装置的气密性:________________________________________。
(2)该同学认为实验Ⅰ可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?__________(填“可行”或“不可行”),原因是_______________________。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是____________________________________,
打开开关K,产生的气体经验纯后点燃,现象是______________________________。
(4)实验Ⅱ中量气管中的液体最好是________(填字母编号,下同)。
a.浓NaOH溶液 b.氨水
c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需要吸收处理。以下各种尾气吸收装置中,适用于吸收NH3,而且能防止倒吸的有____________________________________________________________。


(5)本实验需对量气管进行多次读数,读数时应注意:①将实验装置恢复到室温,②__________________,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况下的体积,忽略滴入的液体体积对气体体积的影响):
| 编号 | 镁铝合金 质量 | 量气管 第一次读数 | 量气管 第二次读数 |
| ① | 1.0 g | 350.0 mL | 13.7 mL |
| ② | 1.0 g | 350.0 mL | 25.0 mL |
| ③ | 1.0 g | 350.0 mL | 14.3 mL |
根据表中数据,可计算出镁铝合金中铝的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
只含C、H两种元素的有机物X、Y,若X中含C质量分数为75%,Y中含C质量分数为85.7%,则X、Y的分子式可能是
A.CH4、C2H4 B.CH4、C2H6 C.C2H4、C2H6 D.CH4、C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A. 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ·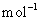 ,则
,则
 的
的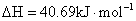
B. 已知MgCO3的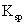 =6.82×
=6.82×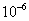 ,则所有含有固体MgCO3的溶液中,都有
,则所有含有固体MgCO3的溶液中,都有
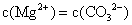 ,且
,且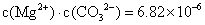
C. 已知:
| 共价键 | C—C | C=C | C—H | H—H |
| 键能/ | 348 | 610 | 413 | 436 |
则可以计算出反应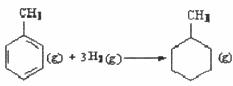 的
的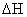 为
为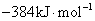
D. 常温下,在0.10 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离程度降低,溶液的pH减小
的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离程度降低,溶液的pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com