
| ŠņŗÅ | V£ØH2SO4£©/mL | c£ØH2SO4£©/mol•L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 3 | t2 |

·ÖĪö øł¾Ż¼ģ²éĘųĆÜŠŌµÄ·½·Ø½ųŠŠ·ÖĪöÅŠ¶Ļ£»
t1£¾t2£¬ĖµĆ÷ŹµŃé¢ņ·“Ó¦ĖŁĀŹ½Ļ“󣬽įŗĻÅØ¶ČµÄÓ°ĻģÅŠ¶Ļ£»
¢Ł¾ŻFe+H2SO4=FeSO4+H2”ü£¬¶ųĒŅ·ÅČČ·ÖĪö£»
¢ŚÕż¼«·¢ÉśµÄ·“Ó¦ĪŖO2+4e-+4OH-=2H2O£¬ĒŅ·“Ó¦·ÅČČ¾Ż“Ė½ųŠŠŌ¤²ā£»·¢ÉśĪüŃõøÆŹ“ĻūŗÄŃõĘų£¬ĘųĢå·Ö×ÓŹż¼õŠ”£®
½ā“š ½ā£ŗ”¾ŹµŃéŅ»”æÓÉŹµŃé×°ÖĆ·ÖĪöµĆ¼ģ²éĘųĆÜŠŌµÄ·½·ØŹĒ“ÓĮæĘų¹ÜÓŅ²ą¹ÜæŚ¼ÓĖ®ÖĮ×óÓŅĮ½¹Ü³öĻÖŅŗĆęøß¶Č²īŹ±Ķ£Ö¹¼ÓĖ®£¬Čō½Ļ³¤Ź±¼äÄܱ£³ÖŅŗĆęøß¶Č²ī²»±ä£¬ŌņĖµĆ÷×°ÖĆĘųĆÜŠŌŗĆ£¬
¹Ź“š°øĪŖ£ŗ“ÓĮæĘų¹ÜÓŅ²ą¹ÜæŚ¼ÓĖ®ÖĮ×óÓŅĮ½¹Ü³öĻÖŅŗĆęøß¶Č²īŹ±Ķ£Ö¹¼ÓĖ®£¬Čō½Ļ³¤Ź±¼äÄܱ£³ÖŅŗĆęøß¶Č²ī²»±ä£¬ŌņĖµĆ÷×°ÖĆĘųĆÜŠŌŗĆ£»
t1£¾t2£¬ĖµĆ÷ŹµŃé¢ņ·“Ó¦ĖŁĀŹ½Ļ“󣬶žÕßÅØ¶Č²»Ķ¬£¬ĖµĆ÷ŌŚĘäĖüĢõ¼žŅ»¶ØŹ±£¬»Æѧ·“Ó¦ĖŁĀŹĖę·“Ó¦ĪļÅØ¶ČµÄŌö“ó¶ųŌö“ó£¬
¹Ź“š°øĪŖ£ŗŌŚĘäĖüĢõ¼žŅ»¶ØŹ±£¬»Æѧ·“Ó¦ĖŁĀŹĖę·“Ó¦ĪļÅØ¶ČµÄŌö“ó¶ųŌö“ó£»
”¾ŹµŃ鶞”æ¢ŁFe+H2SO4=FeSO4+H2”ü£¬ÓŠĘųĢåÉś³É£¬¶ųĒŅ·ÅČČ£¬¹ŹŃ¹ĒæŌö¼Ó£¬¹Ź×ó²ąŅŗĆęĻĀ½µ£»ÓŅ²ąŅŗĆęÉĻÉż£»
¹Ź“š°øĪŖ£ŗĻĀ½µ£»ÉĻÉż£»
¢ŚÕż¼«·¢ÉśµÄ·“Ó¦ĪŖO2+4e-+4OH-=2H2O£¬ĒŅ·“Ó¦·ÅČČ£¬Ō¤²āĮæĘų¹ÜÖŠ³öĻÖµÄĻÖĻóŹĒ£ŗĪüŃõøÆŹ“ĻūŗÄŃõĘų£¬·“Ó¦·ÅČČŹ¹ĘųĢåĪĀ¶ČÉżøߣ¬ČŻĘ÷ÄŚŃ¹ĒæĒ”ŗĆ²»±ä£¬ŅŗĆęƻӊɿ½µ£»Źµ¼Ź¹Ū²ģµ½µÄĻÖĻóæÉÄÜÓėŌ¤²ā²¢²»Ņ»ÖĀ£¬×°ÖĆĘųĆÜŠŌĮ¼ŗĆ£¬ŌŅņŹĒ·¢ÉśĪüŃõøÆŹ“ĻūŗÄŃõĘų£¬ĘųĢå·Ö×ÓŹż¼õŠ”£¬
¹Ź“š°øĪŖ£ŗĪüŃõøÆŹ“ĻūŗÄŃõĘų£¬·“Ó¦·ÅČČŹ¹ĘųĢåĪĀ¶ČÉżøߣ¬ČŻĘ÷ÄŚŃ¹ĒæĒ”ŗĆ²»±ä£¬ŅŗĆęƻӊɿ½µ£»·¢ÉśĪüŃõøÆŹ“ĻūŗÄŃõĘų£¬ĘųĢå·Ö×ÓŹż¼õŠ”£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģŅņĖŲ£¬øÖĢśµÄµē»ÆѧøÆŹ“£¬ÄŃ¶Č²»“ó£¬×¢ŅāÖŖŹ¶µÄ¹éÄÉŗĶŹįĄķŹĒ¹Ų¼ü£®


 ĆūÅĘѧŠ£·Ö²ćÖÜÖܲāĻµĮŠ“š°ø
ĆūÅĘѧŠ£·Ö²ćÖÜÖܲāĻµĮŠ“š°ø »ĘøŌŗ£µķČ«³ĢÅąÓŲāŹŌ¾ķĻµĮŠ“š°ø
»ĘøŌŗ£µķČ«³ĢÅąÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 14.3g | B£® | 25.4g | C£® | 28.6g | D£® | 50.6g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+ | B£® | H2O | C£® | F | D£® | Ne |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶųĀē·ÉĖŁ·¢Õ¹£¬µĆŅęÓŚ¹āĻĖĮ¼ŗƵĵ¼µēŠŌ£¬¹āĻĖµÄÖ÷ŅŖ³É·ÖŹĒøß“æ¶ČµÄ¶žŃõ»Æ¹č | |
| B£® | ¹ÅÓŠ”°ģiŻļŅ»ĪÕ£¬ŅŌĖ®¶žÉżn£¬½ŹČ”Ö”±£¬½ńÓĆŅŅĆŃ“Ó»Ę»ØŻļÖŠĢįČ”ģiŻļĖŲŹĒĄūÓĆŃõ»Æ»¹Ō·“Ó¦ŌĄķ | |
| C£® | ÓĆK2FeO4“śĢęCl2“¦ĄķŅūÓĆĖ®£¬¼Čӊɱ¾śĻū¶¾×÷ÓĆ£¬ÓÖÓŠ¾»Ė®×÷ÓĆ | |
| D£® | ĻĖĪ¬ĖŲ×÷ĪŖÓŖŃųĪļÖŹ£¬ŌŚČĖĢåÄŚ²»¶Ļ·Ö½ā£¬×īÖÕÉś³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼ÅųöĢåĶā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖĪĮĘű¼²µÄĒąŻļĖŲ£ØČēĶ¼£©£¬·Ö×ÓŹ½ĪŖC15H20O5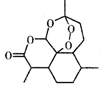 | |
| B£® | ¼×±½±½»·ÉĻµÄŅ»øöĒāŌ×Ó±»-C3H6ClČ”“ś£¬ŠĪ³ÉµÄĶ¬·ÖŅģ¹¹ĢåÓŠ9ÖÖ | |
| C£® | ¶ŌČżĮŖ±½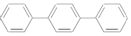 ·Ö×ÓÖŠÖĮÉŁÓŠ16øöŌ×Ó¹²Ę½Ćę ·Ö×ÓÖŠÖĮÉŁÓŠ16øöŌ×Ó¹²Ę½Ćę | |
| D£® | ÓĶÖ¬ŗĶŅŅĻ©ŌŚŅ»¶ØĢõ¼žĻĀ¶¼ÄÜÓėĖ®·“Ó¦£¬ĒŅ·“Ó¦ĄąŠĶĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŽ·ØÅŠ¶ĻŹĒÄÄŅ»ĄąŌŖĖŲ | B£® | Ņ»¶ØŹĒĻ”ÓŠĘųĢåŌŖĖŲ | ||
| C£® | Ņ»¶ØŹĒ¹ż¶ÉŌŖĖŲ | D£® | Ņ»¶ØŹĒ½šŹōŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+ | B£® | F- | C£® | Al3+ | D£® | S2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć¾·Ū | B£® | Ģś·Ū | C£® | Š”ĖÕ“ņ | D£® | ĪŽĖ®ĮņĖįĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
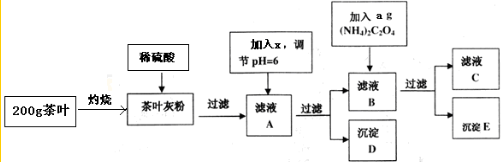
| Ąė×Ó | Ca2+ | Fe3+ |
| ĶźČ«³ĮµķŹ±µÄpH | 13 | 4.1 |
| ±ąŗÅ | ÖÕµćŹ±ĻūŗÄKMnO4ČÜŅŗĢå»ż£ØmL£© |
| 1 | 19.98 |
| 2 | 22.00 |
| 3 | 20.02 |
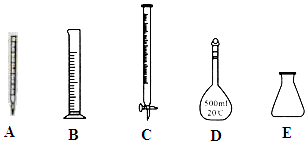
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com