
分析 根据n=$\frac{m}{M}$计算出二氧化碳的物质的量,二氧化碳分子中含有22个质子,据此计算出二氧化碳含有质子的物质的量;根据V=nVm计算出标准状况下二氧化碳的体积.
解答 解:22g二氧化碳的物质的量为:$\frac{22g}{44g/mol}$=0.5mol,0.5mol二氧化碳分子中含有质子的物质的量为:0.5mol×22=11mol;
标准状况下0.5mol二氧化碳在标准状况下的体积为:22.4L/mol×0.5mol=11.2L,
故答案为:0.5;11;11.2.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的 化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| B. | c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+) | |
| D. | c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为34,质子数为29的铜原子:${\;}_{34}^{63}$Cu | |
| B. | 碳原子的结构示意图: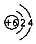 | |
| C. | 二氧化碳的电子式: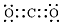 | |
| D. | 乙醇的结构简式:CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
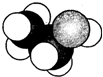 图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“
图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“ ”表示氧原子,该有机物的结构简式是( )
”表示氧原子,该有机物的结构简式是( )| A. | CH3CH3 | B. | CH2=CH2 | C. | CH3COOH | D. | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量NaOH固体时动作缓慢 | B. | 定容时俯视刻度线 | ||
| C. | 定容后振荡发现液面低于刻度线 | D. | 未洗涤烧杯和玻璃棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学能帮助我们更好地认识生活、改善生活.
化学能帮助我们更好地认识生活、改善生活.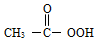 )易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.
)易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com