
科目:高中化学 来源: 题型:解答题
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 人体内含量最多的元素,且其单质是常见的助燃剂. | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. | 第三周期元素的简单离子中半径最小 |
 ;写出元素X的气态氢化物的电子式
;写出元素X的气态氢化物的电子式 ;离子半径比较:Y离子>Z离子(填“>”或“<”).
;离子半径比较:Y离子>Z离子(填“>”或“<”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有机物X的键线式为:
有机物X的键线式为: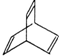
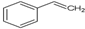
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅由碳元素组成的物质一定是纯净物 | |
| B. | C60是碳的一种同素异形体 | |
| C. | C60的摩尔质量是720g | |
| D. | 石墨转变为金刚石不属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②③④⑤ | C. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应在不加热的条件下一定不能发生 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 由“100KPa时石墨转化为金刚石,要吸收1.895kJ的热能”可知在100KPa压强下石墨比金刚石稳定 | |
| D. | 化学反应中的能量变化,只表现为热能的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100ml~120ml | B. | 100ml~120ml | C. | 110ml~130ml | D. | 100ml~130ml |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com