
����Ŀ���мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾���þƬ����Ƭ���缫������ͬѧ���缫����6 mol��L��1��H2SO4��Һ�У���ͬѧ���缫����6 mol��L��1��NaOH��Һ�У���ͼ��ʾ��

��1��д�����������ĵ缫��Ӧʽ___________________��
��2�����и�������Ϊ___________________�������ܷ�Ӧ�����ӷ���ʽ��___________________��
��3��������ͬѧ����Ϊ���������ԭ��صĵ缫���϶��ǽ������ɸ������ϵĽ���Ӧ�ȹ����������ϵĽ���������������жϳ�___________________��Ը�ǿ�����һ��жϳ�___________________��Ը�ǿ(��дԪ�ط���)��
��4���ɴ�ʵ��ó������н����У���ȷ����___________________��
A������ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ���
B��þ�Ľ����Բ�һ�������Ľ�����ǿ
C����ʵ��˵���������˳����ѹ�ʱ��û��ʵ�ü�ֵ��
D����ʵ��˵����ѧ�о������ӣ���Ӧ������Ӱ��ϴ����Ӧ��������������
���𰸡� 2H����2e��===H2�� Al 2Al��2OH����2H2O===2AlO![]() ��3H2�� Mg Al AD
��3H2�� Mg Al AD
����������1���׳��л��ý���þ�����������������������ĵ缫��Ӧʽ��2H++2e-=H2������2���ҳ�����������������Һ������Ӧ���������������ĵ缫��ӦʽΪAl+4OH--3e-=AlO2��+2H2O���ܷ�Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O=2AlO2��+3H2������3������ס���ͬѧ����Ϊ������ԭ��صĵ缫����������ǽ������ɸ������ϵĽ���Ӧ�ȹ����������ϵĽ������ã�����жϳ�Mg��Ը�ǿ�����һ��жϳ�Al��Ը�ǿ����4��A.�������Ϸ�����֪����ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ��ʣ�A��ȷ��B.þ�Ľ�����һ�������Ľ�����ǿ��B����C.�������˳���DZ���֤�ķ�Ӧ���ɣ������ʱ�����кܴ�ʹ�ü�ֵ��C����D.��ʵ��˵����ѧ�о������ӣ���Ӧ������Ӱ��ϴ����Ӧ����������������D��ȷ����ѡAD��


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Һ��������������ռ���Һ��װ������ͼ��ʾ������������������Ϊ��������缫�����ͬ��ͬѹ�£�������������ҵ������ԼΪ1��2������˵����ȷ����
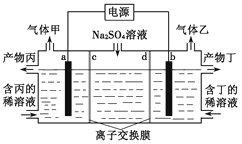
A. a�����Դ�ĸ�������
B. ���ﶡΪ������Һ
C. ���ӽ���ĤdΪ�����ӽ���Ĥ(����������ͨ��)
D. b�缫����ʽΪ2H2O+2e-=2OH-+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪298Kʱ��ij��MOH�ĵ���ƽ�ⳣ��Kb=1.0��10-5�������a=![]() ����20.00mL0.1000mol/LMOH��Һ�еμ�0.10mol/L���ᣬ�����Һ��pH���¶����������������Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
����20.00mL0.1000mol/LMOH��Һ�еμ�0.10mol/L���ᣬ�����Һ��pH���¶����������������Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
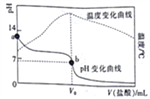
A. a���Ӧ����Һ��:c(OH-)=(M+)+<(H+)
B. b���Ӧ��V��=20.00mL
C. 298Kʱ��0.1000mol/LMOH��Һ�У�MOH�ĵ����a=1%
D. 298Kʱ����0.1molMOH��0.1moMCl����ˮ���Ƴ�1L�����Һ����Һ��pH>9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����ۼס��ҡ���������������װ�õ��й��÷������в��������ǣ� �� 
A.��װ�ã�������֤��̼�ķǽ����Աȹ�ǿ
B.��װ�ã���Ƥ�ܵ���������ʹˮ˳������
C.��װ�ã���ͼʾ�ķ������ܼ���װ�õ�������
D.��װ�ã��ȴӢٿڽ�������������̼���ٴӢڿڽ��������ռ�һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ���������Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ������˵����ȷ����

A. a�ĵ����ڸ������������û���e�ĵ�����˵���ǽ�����a��e
B. b��d����Ԫ�صļ����Ӱ뾶�����ǰ�߽ϴ�
C. ��b��e����Ԫ����ɵĻ��������ܽ���ǿ����Һ��������������Һ��Ӧ
D. ��c��d�ֱ���f��ɵĻ������еĻ�ѧ��������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������У��������Ȳ���������Ȼ��������ܽ����������
����ʯ��ˮ����ͨ��CO2ֱ������
����CaCl2�ܲ�����ͨ��CO2ֱ������
����Ba(OH)2��Һ����μ���ϡ����ֱ������
����Fe(OH)3��������μ���ϡ����ֱ������
A. �٢� B. �٢ڢ� C. �ڢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʷ�����ȷ����
�� | �� | �� | ������ | |
A | ���� | ���� | ������ | �ɱ� |
B | ������ | �ռ� | ���� | ����ͭ |
C | ̼�� | ��ʯ�� | С�մ� | �������� |
D | ������̼ | ������ | ʳ�� | ʯ��ʯ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��1����һ�鴿����пƬ����ʢ��ϡ������ձ��У��ɹ۲쵽пƬ���ܽ⣬�������ݲ�����ƽ�еز���һ��ͭƬ(��ͼ��װ����ʾ)���ɹ۲쵽ͭƬ��________(������������û����)���ݲ��������õ��߰�пƬ��ͭƬ��������(��ͼ��װ����ʾ)���ɹ۲쵽ͭƬ��________(������������û����)���ݲ�����
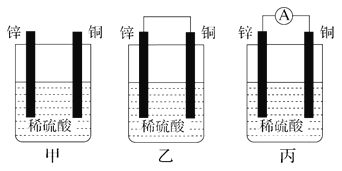
��2���õ��߽�����������������Һ�е�пƬ��ͭƬ����(��ͼ��װ����ʾ)���۲쵽��������ָ�뷢����ƫת��˵���������е���ͨ����пƬ�ϵĵ缫��Ӧ��______________��ͭƬ�ϵĵ缫��Ӧ��____________________________��
��3���ҡ���װ���ǽ�________��ת��Ϊ________�ܵ�װ�á�
�����Ͽ�1molH��H����1molN��H����1molN��N���ֱ���Ҫ���յ�����Ϊ436kJ��391kJ��946kJ����
��1��1molN2����NH3��_____�����������������ų���������_____ kJ
��2��1molH2����NH3��_____�����������������ų���������_____ kJ�������ǿ��淴Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���CH3CH2CH2CH3��CH3CH��CH3��2�Ĺ�ϵ�ǣ�������
A.��Ϊͬλ��
B.��Ϊͬϵ��
C.��Ϊͬ���칹��
D.��Ϊͬ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com