
己知:|||+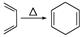 ,如果要合成
,如果要合成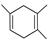 ,所用的起始原料可以是
,所用的起始原料可以是
①2甲基1,3丁二烯和2丁炔 ②1,3戊二烯和2丁炔 ③2,3二甲基1,3戊二烯和乙炔 ④2,3二甲基1,3丁二烯和丙炔
| A.①④ | B.②③ | C.①③ | D.②④ |
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 3 |
| 2 |

| c4(H2O) |
| c4(H2) |
| c4(H2O) |
| c4(H2) |
查看答案和解析>>
科目:高中化学 来源:2010~2011学年浙江省台州市高一下学期期末考试化学 题型:填空题
(12分)I:能源是人类生活和社会发展的基础,地球上最基本的能源是 ▲ ,大自然利用这一能源最成功的是 ▲ 。氢气被人们看作理想的绿色能源,己知氢气的热值是143kJ·g-1(热值指的是在一定条件下单位质量的物质完全燃烧所放出的热量,氢气转化为液态水。)请写出氢气燃烧的热化学方程式 ▲ 。
Ⅱ:理论上任意一个自发的氧化还原反应都能设计成原电池,现有如下反应:
2FeCl3 + Cu = 2FeCl2 + CuCl2
如果将其设计成原电池,请写出负极材料及正极电极反应式。
负极材料: ▲ ;正极电极反应式: ▲ 。
III:工业上用电解熔融氧化铝的方法制取金属铝。
(1)请写出工业用电解熔融氧化铝制取铝的化学方程式: ▲ 。
(2)现冶炼2.7 t 铝,需要转移电子的物质的量为 ▲ mol。
查看答案和解析>>
科目:高中化学 来源:2013届贵州省高二下学期第一次月考化学试卷(解析版) 题型:选择题
己知:|||+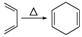 ,如果要合成
,如果要合成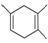 ,所用的起始原料可以是
,所用的起始原料可以是
①2甲基1,3丁二烯和2丁炔 ②1,3戊二烯和2丁炔 ③2,3二甲基1,3戊二烯和乙炔 ④2,3二甲基1,3丁二烯和丙炔
A、①④ B.②③ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com