
分析 (1)当硬水中钙和镁主要以碳酸氢盐,如Ca(HCO3)2、Mg(HCO3)2形式存在时,称为暂时硬水,当这种硬水加热煮沸时,碳酸氢盐会转化为沉淀除去;如果硬水中钙和镁主要以硫酸盐或氯化物等形式存在,则称为永久硬水,它们不能用煮沸的方法除去;
(2)以硫酸盐或氯化物形式存在时所引起的硬度,则称为永久硬度,加入石灰水只能降低Mg2+所形成的永久硬度,但转变为Ca2+形成的永久硬度,加石灰水发生:Ca(OH)2+Ca(HCO3)2=2CaCO3↓+2H2O,2Ca(OH)2+Mg(HCO3)2=2CaCO3↓+Mg(OH)2↓+2H2O,只能降低暂时硬度,不能降低永久硬度,把部分Mg2+所形成的永久硬度转变为Ca2+形成的永久硬度;
(3)取自江河湖泊中的淡水的处理顺序是:先沉淀、再过滤,最后消毒处理;
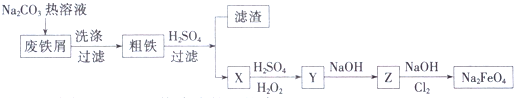
(4)由流程图和实验目的可知,用工业废铁屑(含铜、碳、硅等)制取高铁酸钠,其中X、Y、Z是含铁化合物,碳酸钠溶液水解显碱性,洗涤废铁屑表面油污,油脂在碱性溶液中水解生成溶于水的物质得到粗铁,加入硫酸,铁和硫酸反应生成硫酸亚铁,过滤得到滤渣为铜和硅,滤液为硫酸亚铁,加入硫酸和过氧化氢氧化亚铁离子为铁离子,加入氢氧化钠用生成氢氧化铁沉淀,在氢氧化钠溶液中通入氯气生成高铁酸钠;
①碳酸钠溶液水解显碱性清除废铁屑表面的油污;
②X为硫酸亚铁,Y为硫酸铁,硫酸亚铁加入过氧化氢和硫酸发生氧化还原反应;
③Z为氢氧化铁,在氢氧化钠溶液中氯气氧化氢氧化铁为高铁酸钠,依据原子守恒和氧化还原反应电子守恒配平书写化学方程式;
④高铁酸钠具有强氧化性能杀菌消毒,在反应过程中被还原为铁离子在水溶液中水解生成氢氧化铁胶体,胶体具有吸附悬浮杂质的作用起到净水作用;
⑤电解时阳极发生氧化反应,铁失电子生成高铁酸根离子,由电解质溶液电荷守恒配平写出电极反应方程式.
解答 解:(1)当硬水中钙和镁主要以碳酸氢盐,如Ca(HCO3)2、Mg(HCO3)2形式存在时,称为暂时硬水,当这种硬水加热煮沸时,碳酸氢盐会转化为沉淀除去;如果硬水中钙和镁主要以硫酸盐或氯化物等形式存在,则称为永久硬水,它们不能用煮沸的方法除去,但药剂法、离子交换法均可将钙和镁离子浓度减小,降低硬度,
故答案为:bc;
(2)a.以硫酸盐或氯化物形式存在时所引起的硬度,则称为永久硬度,加入石灰水只能降低Mg2+所形成的永久硬度,但转变为Ca2+形成的永久硬度,故a错误;
b.加石灰水发生:Ca(OH)2+Ca(HCO3)2=2CaCO3↓+2H2O,2Ca(OH)2+Mg(HCO3)2=2CaCO3↓+Mg(OH)2↓+2H2O,只能降低暂时硬度,不能降低永久硬度,故b误;
c.加石灰水发生反应:MgSO4+Ca(OH)2=Mg(OH)2↓+CaSO4; MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2,把部分Mg2+所形成的永久硬度转变为Ca2+形成的永久硬度,故c错误;
d.由c分析可知,加石灰水把部分Mg2+所形成的永久硬度转变为Ca2+形成的永久硬度,故d正确;
故答案为:d;
(3)取自江河湖泊中的淡水的处理顺序是:先沉淀、再过滤,最后消毒处理,故答案为:混凝沉淀→过滤→杀菌消毒;
(4)由流程图和实验目的可知,用工业废铁屑(含铜、碳、硅等)制取高铁酸钠,其中X、Y、Z是含铁化合物,碳酸钠溶液水解显碱性,洗涤废铁屑表面油污,油脂在碱性溶液中水解生成溶于水的物质得到粗铁,加入硫酸,铁和硫酸反应生成硫酸亚铁,过滤得到滤渣为铜和硅,滤液为硫酸亚铁,加入硫酸和过氧化氢氧化亚铁离子为铁离子,加入氢氧化钠用生成氢氧化铁沉淀,在氢氧化钠溶液中通入氯气生成高铁酸钠;
①废铁屑中加入Na2CO3热溶液的目的为清洗废铁屑表面的油污,故答案为:清洗废铁屑表面的油污;
②X为硫酸亚铁,Y为硫酸铁,X转化为Y的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
③Z为氢氧化铁,在氢氧化钠溶液中氯气氧化氢氧化铁为高铁酸钠,Cl2将Z氧化为Na2FO4 的化学方程式为10NaOH+3Cl2+2Fe(OH)3═2Na2FeO4+6NaCl+8H2O,
故答案为:10NaOH+3Cl2+2Fe(OH)3═2Na2FeO4+6NaCl+8H2O;
④高铁酸钠消毒后的还原产物具有净水作用,其净水原理高铁酸盐在杀菌消毒时,本身被还原成Fe3+,Fe3+易水解生成Fe(OH)3,具有胶体的性质,可吸附水中的悬浮杂质,而起到净化水的作用为,故答案为:高铁酸盐在杀菌消毒时,本身被还原成Fe3+,Fe3+易水解生成Fe(OH)3,具有胶体的性质,可吸附水中的悬浮杂质,而起到净化水的作用;
⑤电解时阳极发生氧化反应,铁失电子生成高铁酸根离子,由电解质溶液配平电荷守恒可知电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O,故答案为:Fe+8OH--6e-═FeO42-+4H2O.
点评 本题考查混合物分离提纯及物质制备实验,为高频考点,把握物质的性质、流程中的反应为解答的关键,侧重分析与应用能力的综合考查,题目难度中等.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:选择题
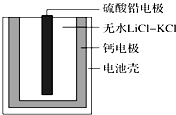 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 正极反应式:Ca+2Cl--2e-=CaCl2 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 常温时,在正负极间接上电流表或检流计,指针发生偏转 | |
| D. | 每转移0.1 mol电子,理论上生成10.35g Pb |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
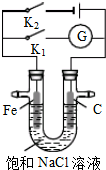
| A. | 只闭合K1,电流计G指针不发生偏转 | |
| B. | 只闭合K1,石墨棒周围溶液pH逐渐降低 | |
| C. | 只闭合K2,电路中通过0.1mol电子时,两极共产生2.24L气体 | |
| D. | 只闭合K2,铁棒上发生的反应为:2H2O+2e-═H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
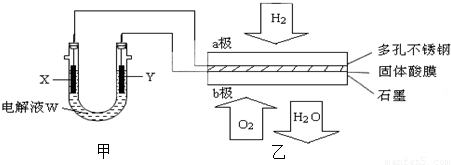
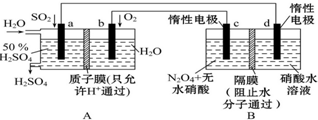 膜技术原理在化工生产中有着广泛的应用.有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5(N2O5极易和水反应),装置如图:
膜技术原理在化工生产中有着广泛的应用.有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5(N2O5极易和水反应),装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40% | B. | 33% | C. | 60% | D. | 36% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
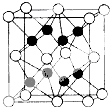 已知:A、D、E、G、J、L、M七种元素的原子序数依次增大.A在所有元素中原子半径最小;D原子核外电子有6种不同运动状态;G与E、J均相邻;A、G、J三种元素的原子序数之和为25;J2-和L+有相同的核外电子排布;M的质子数是25.请回答下列问题:
已知:A、D、E、G、J、L、M七种元素的原子序数依次增大.A在所有元素中原子半径最小;D原子核外电子有6种不同运动状态;G与E、J均相邻;A、G、J三种元素的原子序数之和为25;J2-和L+有相同的核外电子排布;M的质子数是25.请回答下列问题: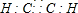 、
、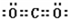 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com