
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中只有C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1、B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题.
(1)A是 ,B是 ,C是 ,E是 .
(2)B在周期表中位于 区.
(3)写出C元素基态原子核外电子排布式, .
(4)用轨道表示式表示D元素原子的价电子构型 .
考点: 位置结构性质的相互关系应用.
分析: A、B、C、D、E5种短周期元素,它们的核电荷数依次增大,且都小于20,B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,最外层电子排布为ns2np4,则B为O元素、D为S元素;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,E的原子序数大于硫,且5种元素中只有C、E是金属元素,则A为H元素、E为K元素;C原子最外层上电子数等于D原子最外层上电子数的一半,其最外层电子数为6×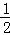 =3,故C为Al,据此解答.
=3,故C为Al,据此解答.
解答: 解:(1)A、B、C、D、E5种短周期元素,它们的核电荷数依次增大,且都小于20,B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,最外层电子排布为ns2np4,则B为O元素、D为S元素;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,E的原子序数大于硫,且5种元素中只有C、E是金属元素,则A为H元素、E为K元素;C原子最外层上电子数等于D原子最外层上电子数的一半,其最外层电子数为6×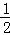 =3,故C为Al,
=3,故C为Al,
故答案为:H;O;Al;K;
(2)B为O元素,最外层电子数排布为2s22p4,处于周期表中p区,故答案为:p;
(3)C为铝元素元素,原子核外有13个电子,基态原子核外电子排布为1s22s22p63s23p1,故答案为:1s22s22p63s23p1;
(4)D为S元素,基态原子最外层电子排布式为3s23p4,其轨道排布式为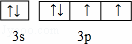 ,故答案为:
,故答案为: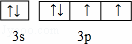 .
.
点评: 本题考查结构位置关系、元素周期表,元素的推断是解答的关键,侧重对核外电子排布的考查,旨在考查学生对基础知识的掌握.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为: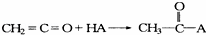 ,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
|
| A. | 与HCl加成生成CH3COCl |
|
| B. | 与H2O加成生成CH3COOH |
|
| C. | 与CH3OH加成生成CH3COCH2OH |
|
| D. | 与CH3COOH加成生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于主族元素电子排布特征的说法正确的是()
A. 主族元素的原子核外电子最后填入的能级是s能级
B. 主族元素的原子核外电子最后填入的能级是s能级或p能级
C. 主族元素的原子核外电子最后填入的能级是d能级或f能级
D. 主族元素的原子核外电子最后填入的能级是s能级或d能级
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,下列物质占体积最大的是()
A. 0.6 g H2 B. 98 g H2SO4
C. 6.02×1022个CO2 D. 4.48 L HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列反应的离子方程式
(1)硫酸氢钠溶液中加入硝酸钡溶液产生白色沉淀: ;
(2)在小苏打(NaHCO3)溶液中加盐酸,有无色气体产生: ;
(3)在200mL的烧杯中加入50mL蒸馏水,加热至沸腾,滴入10滴饱和氯化铁溶液,继续加热至溶液呈红褐色 .
查看答案和解析>>
科目:高中化学 来源: 题型:
Li﹣Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e﹣=Li2S+Fe.有关该电池的下列说法中,正确的是()
A. Li﹣Al在电池中作为负极材料,该材料中Li的化合价为+1价
B. 该电池的电池反应式为:2Li+FeS=Li2S+Fe
C. 负极的电极反应式为Al﹣3e﹣=Al3+
D. 充电时,阴极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com