
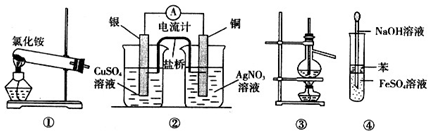
| A. | 实验室用装置①制取氨气 | |
| B. | 装置②将化学能转化为电能 | |
| C. | 装置③可用于分离沸点相差较大的互溶液体混合物 | |
| D. | 装置④可用于 Fe(OH)2的制取,并能防止 Fe(OH)2被氧化 |
分析 A.氯化铵分解后,在试管口又化合生成氯化铵;
B.右侧烧杯中发生Cu与硝酸银的反应,不能构成原电池;
C.温度计测定馏分的温度;
D.苯可隔绝空气,防止生成的氢氧化亚铁被氧化.
解答 解:A.氯化铵分解后,在试管口又化合生成氯化铵,不能制备氨气,应选铵盐与碱共热制备氨气,故A错误;
B.右侧烧杯中发生Cu与硝酸银的反应,不能构成原电池,应将电解质互换,实现将化学能转化为电能,故B错误;
C.温度计测定馏分的温度,则温度计的水银球在蒸馏烧瓶的支管口处,故C错误;
D.苯可隔绝空气,防止生成的氢氧化亚铁被氧化,则图中装置可制备Fe(OH)2,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、混合物分离、物质的制备实验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 在小苏打溶液中:NO3-、AlO2-、NH4+、K+ | |
| B. | 在空气中:H2S、CO2、SO2、CO | |
| C. | 在酸性高锰酸钾溶液中:C2H5OH、Na+、SO42-、CO32- | |
| D. | 在pH=8的溶液中:Na+、HCO3-、Br-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知某可逆反应mA(g)+nB(g)?qD(g)在密闭容器中进行.
已知某可逆反应mA(g)+nB(g)?qD(g)在密闭容器中进行.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
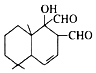 是一种取代有机氯农药DDT的新型杀虫剂.
是一种取代有机氯农药DDT的新型杀虫剂. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 140℃时,无水乙醇与浓硫酸共热可制备乙烯 | |
| B. | 往油脂中加稀硫酸与之共热可发生皂化反应 | |
| C. | 可用碘溶液检验淀粉是否水解完全 | |
| D. | 验证溴乙烷中的溴元素,可直接加AgNO3溶液观察是否有淡黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 失去电子的反应是还原反应 | B. | 发生氧化反应的是氧化剂 | ||
| C. | 作氧化剂的物质不能同时作还原剂 | D. | 失去电子的物质是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.
,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com