
ЎҫМвДҝЎҝAЎўBЎўCЎўDЎўEКЗОеЦЦ¶МЦЬЖЪЦчЧеФӘЛШЈ¬ЖдЦРAКЗФӘЛШЦЬЖЪұнЦРФӯЧУ°лҫ¶ЧоРЎөДФӘЛШЈ»BКЗРОіЙ»ҜәПОпЦЦАаЧо¶аөДФӘЛШЈ»CКЗөШҝЗЦРә¬БҝЧо¶аөДФӘЛШЈ»DөДЖшМ¬Зв»ҜОпөДЛ®ИЬТәПФјоРФЈ»EҪрКфЦЖіЙҪрКф°еәуЈ¬ҫӯјУ№ӨҝЙЦЖіЙТ»ЦЦёЯЦКБҝөД·ҙ№вҫөЈ¬ёГҪрКф·ЫД©әНСх»ҜМъ»мәПіЈУГУЪәёҪУёЦ№мЈ®
(1)РҙіцCЎўEөДФӘЛШ·ыәЕ______Ўў______ЎЈ
(2)BФӘЛШО»УЪЦЬЖЪұнЦРөДО»ЦГОӘ______Ј¬BC2өДөзЧУКҪОӘ______(УГФӘЛШ·ыәЕұнКҫ)ЎЈ
(3)AЎўBЎўCЎўDөДФӯЧУ°лҫ¶УЙҙуөҪРЎөДЛіРтОӘ______(УГФӘЛШ·ыәЕұнКҫ)ЎЈ
(4)EөДЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпУл¶МЦЬЖЪФӘЛШЦРЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпјоРФЧоЗҝөДОпЦКФЪИЬТәЦР·ҙУҰөДАлЧУ·ҪіМКҪ______ЎЈ
Ўҫҙр°ёЎҝO Al өЪ¶юЦЬЖЪIVAЧе ![]() CЈҫNЈҫOЈҫH AlЈЁOHЈ©3+OH©Ғ=AlO2©Ғ+2H2O
CЈҫNЈҫOЈҫH AlЈЁOHЈ©3+OH©Ғ=AlO2©Ғ+2H2O
ЎҫҪвОцЎҝ
AЎўBЎўCЎўDЎўEКЗОеЦЦ¶МЦЬЖЪЦчЧеФӘЛШЈ¬ЖдЦРAКЗФӘЛШЦЬЖЪұнЦРФӯЧУ°лҫ¶ЧоРЎөДФӘЛШЈ¬ФтAОӘHФӘЛШЈ»BКЗРОіЙ»ҜәПОпЦЦАаЧо¶аөДФӘЛШЈ¬ФтBОӘCФӘЛШЈ»CКЗөШҝЗЦРә¬БҝЧо¶аөДФӘЛШЈ¬ФтCОӘOФӘЛШЈ»DөДЖшМ¬Зв»ҜОпөДЛ®ИЬТәПФјоРФЈ¬ФтDОӘNФӘЛШЈ»EҪрКфЦЖіЙҪрКф°еәуЈ¬ҫӯјУ№ӨҝЙЦЖіЙТ»ЦЦёЯЦКБҝөД·ҙ№вҫөЈ¬ёГҪрКф·ЫД©әНСх»ҜМъ»мәПіЈУГУЪәёҪУёЦ№мЈ¬ФтEОӘAlЎЈ
ЈЁ1Ј©CОӘOФӘЛШЎўEОӘAlФӘЛШЈ¬№Кҙр°ёОӘЈәOЈ»AlЈ»
ЈЁ2Ј©BОӘМјФӘЛШЈ¬О»УЪЦЬЖЪұнЦРөДО»ЦГОӘЈәөЪ¶юЦЬЖЪIVAЧеЈ¬CO2өДөзЧУКҪОӘ![]() Ј¬№Кҙр°ёОӘЈәөЪ¶юЦЬЖЪIVAЧеЈ»
Ј¬№Кҙр°ёОӘЈәөЪ¶юЦЬЖЪIVAЧеЈ»![]() Ј»
Ј»
ЈЁ3Ј©ЛщУРФӘЛШЦРHФӯЧУ°лҫ¶ЧоРЎЈ¬Н¬ЦЬЖЪЧФЧу¶шУТФӯЧУ°лҫ¶јхРЎЈ¬№КФӯЧУ°лҫ¶ЈәCЈҫNЈҫOЈҫHЈ¬№Кҙр°ёОӘЈәCЈҫNЈҫOЈҫHЈ»
ЈЁ4Ј©EөДЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпОӘAlЈЁOHЈ©3Ј¬¶МЦЬЖЪФӘЛШЦРЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпјоРФЧоЗҝөДОпЦКОӘNaOHЈ¬¶юХЯФЪИЬТәЦР·ҙУҰөДАлЧУ·ҪіМКҪЈәAlЈЁOHЈ©3+OH©Ғ=AlO2©Ғ+2H2OЈ¬
№Кҙр°ёОӘЈәAlЈЁOHЈ©3+OH©Ғ=AlO2©Ғ+2H2OЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝіЈОВПВЈ¬Пт20 mLДіЕЁ¶ИөДБтЛбИЬТәЦРөОИл0.1 molЎӨLЈӯ1°ұЛ®Ј¬ИЬТәЦРЛ®өзАліцөДЗвАлЧУЕЁ¶ИЛжјУИл°ұЛ®өДМе»эұд»ҜИзНјЛщКҫЎЈПВБР·ЦОцХэИ·өДКЗ
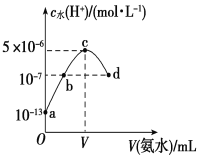
A.cөгЛщКҫИЬТәЦРЈәc(HЈ«)Јӯc(OHЈӯ)ЈҪc(NH3ЎӨH2O)
B.bөгЛщКҫИЬТәЦРЈәc(NH4Ј«)ЈҪ2 c(SO42Јӯ)
C.VЈҪ40
D.ёГБтЛбөДЕЁ¶ИОӘ0.1 molЎӨLЈӯ1
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ№ӨТөЙПУЙГәМҝіц·ўЦЖИЎУР»ъ»Ҝ№ӨФӯБПТТИІЈ¬БчіМИзПВЎЈ»ШҙрТФПВОКМвЈә
![]()
(1)УЙГәМҝөГөҪҪ№МҝөД№ӨТөІЩЧчОӘ_____________ЎЈ
aЈ®·ЦБу bЈ®ёЙБу cЈ®БС»Ҝ dЈ®БСҪв
(2)КөСйКТУГөзКҜЈЁCaC2Ј©АҙЦЖұёТТИІЈ¬·ҙУҰөД»ҜС§·ҪіМКҪОӘЈә___________ЎЈТТИІКЗТ»ЦЦЙФУРЖшО¶өДЖшМеЈ¬ө«КөСйКТЦЖұёөДТТИІЖшМеҫЯУРБоИЛСб¶сөДҙМјӨРФЖшО¶Ј¬ҝЙУГДіЦЦИЬТәҪшРРјмСйЈ¬РҙіцјмСйҙЛЖшМеөД»ҜС§·ҪіМКҪЈә___________
(3)ТТИІДЬК№деЛ®НКЙ«Ј¬ЛөГчТТИІ·ўЙъ_____________·ҙУҰЈЁ·ҙУҰАаРНЈ©Ј»ТТИІДЬК№ЛбРФёЯГМЛбјШНКЙ«Ј¬ЛөГчТТИІИЭТЧұ»_____________ЎЈөјөзёЯ·ЦЧУКЗТФҫЫТТИІОӘФШМеөДёЯҫЫОпЈ¬Рҙіц·ҙУҰўтөД»ҜС§·ҪіМКҪЈә_____________ЎЈ
(4)ТТИІФЪТ»¶ЁМхјюПВЈ¬ИэҫЫөГөҪCH2©„CHЎӘCЎФCЎӘCH©„CH2ЈәЈ¬РҙіцёГИэҫЫОпҫЯУРПаН¬»ҜС§КҪЗТІ»ТЧ·ўЙъјУіЙ·ҙУҰОпЦКөДҪб№№јтКҪЈә_________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝH3AsO3УлSnCl2ФЪЕЁСОЛбЦР·ҙУҰөДАлЧУ·ҪіМКҪОӘ3Sn2Ј«Ј«2H3AsO3Ј«6HЈ«Ј«18ClЈӯ=2AsЈ«3SnCl62ЈӯЈ«6MЎЈ№ШУЪёГ·ҙУҰөДЛө·ЁЦРҙнОуөДКЗ
A.MОӘH2O
B.»№ФӯјБКЗSn2Ј«Ј¬»№ФӯІъОпКЗAs
C.Сх»ҜРФЈәH3AsO3ЈҫSnCl62Јӯ
D.ГҝЙъіЙ7.5 g AsЈ¬ЧӘТЖөДөзЧУОӘ0.6 mol
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝPCl3ЦчТӘУГУЪЦЖФмөР°ЩіжөИУР»ъБЧЕ©Т©әН»З°·аЧаӨ(S.D)өИТҪТ©өДФӯБПЎЈИзНјОӘКөСйКТЦРЦЖИЎҙЦPCl3ІъЖ·өДЧ°ЦГЈ¬јРіЦЧ°ЦГВФИҘЎЈ
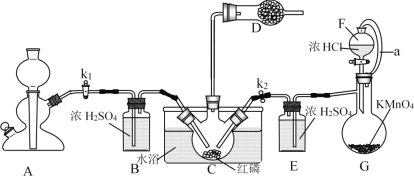
ҫӯІйФДЧКБПЦӘЈәәмБЧУлЙЩБҝCl2·ҙУҰЙъіЙPCl3Ј¬Ул№эБҝCl2·ҙУҰЙъіЙPCl5ЎЈPCl3УцЛ®»бЗҝБТЛ®ҪвЙъіЙH3PO3ЎЈPCl3УцO2»бЙъіЙPOCl3(ИэВИСхБЧ)Ј¬PCl3ЎўPOCl3өДИЫ·РөгјыПВұнЎЈ
ОпЦК | ИЫөг/Ўж | ·Рөг/Ўж |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
»ШҙрПВБРОКМвЈә
(1)ТЗЖчGөДГыіЖКЗ______ЎЈЧ°ЦГFУлGУЙПрҪә№ЬaПаБ¬НЁЈ¬aөДЧчУГКЗ_______ЎЈ
(2)AКЗЦЖИЎCO2Ч°ЦГЈ¬CO2өДЧчУГКЗ_____Ј¬СЎФсAЦРөДТ©Ж·КЗ_____(МоЧЦДё)ЎЈ
a.ПЎСОЛб b.ПЎБтЛб c.NaHCO3·ЫД© d.ҝйЧҙКҜ»ТКҜ
(3)Ч°ЦГDЦРКўУРјоКҜ»ТЈ¬ЖдЧчУГКЗ__________________ЎЈ
(4)Ч°ЦГGЦРЙъіЙCl2Ј¬·ҙУҰөДАлЧУ·ҪіМКҪОӘ___________ЎЈ
(5)Ч°ЦГCІЙУГ65-70ЎжЛ®ФЎјУИИЈ¬ЦЖөГөДPCl3ҙЦІъЖ·ЦРіЈә¬УРPOCl3ЎўPCl5өИФУЦКЈ¬іэФУөД·Ҫ·ЁКЗЈәПИјУИләмБЧјУИИЈ¬іэИҘPCl5Ј¬И»әуНЁ№э___________(МоКөСйІЩЧчГыіЖ)Ј¬јҙҝЙөГөҪҪПҙҝҫ»өДPCl3ЎЈ
(6)НЁ№эКөСйІв¶ЁҙЦІъЖ·ЦРPCl3өДЦКБҝ·ЦКэЈ¬КөСйІҪЦиИзПВ(І»ҝјВЗФУЦКөД·ҙУҰ)Јә
өЪТ»ІҪЈәСёЛЩТЖИЎ20.0 g PCl3ҙЦІъЖ·Ј¬јУЛ®НкИ«Л®ҪвәуЈ¬ФЩЕдіЙ500mLИЬТәЈ»
өЪ¶юІҪЈәТЖИЎ25.00mLИЬТәЦГУЪЧ¶РОЖҝЦРЈ»
өЪИэІҪЈәјУИл0. 5molLЈӯ1өвИЬТә20mLЈ¬өв№эБҝЈ¬H3PO3НкИ«·ҙУҰЙъіЙH3PO4Ј»
өЪЛДІҪЈәјУИлјёөОөн·ЫИЬТәЈ¬УГ1.0 molLЈӯ1Na2S2O3ұкЧјИЬТәөО¶Ё№эБҝөДөвЈ¬·ҙУҰ·ҪіМКҪОӘI2+2Na2S2O3=Na2S4O6+2NaIЈ¬өОЦБЦХөгКұПыәДNa2S2O3ұкЧјИЬТә12mLЎЈ
ўЩөЪИэІҪЦР·ҙУҰөД»ҜС§·ҪіМКҪОӘ_____________ЎЈ
ўЪёщҫЭЙПКцКэҫЭЈ¬јЖЛгёГІъЖ·ЦРPCl3өДЦКБҝ·ЦКэОӘ______%ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ0.78ҝЛГҫВБөД»мәПОпН¶ИлөҪ25mL30.625%ПЎБтЛб(ГЬ¶ИОӘ1.28g/cm3)ЦРЈ¬ід·Ц·ҙУҰЈ¬ФЪұкЧјЧҙМ¬ПВөГөҪЖшМеМе»э0.896L(ЖшМе»щұҫЙПИ«ІҝКХјҜ)Ј¬ФЪ·ҙУҰәуөДИЬТәЦРјУИл4mol/L NaOHИЬТәЈ¬К№ГҫАлЧУНкИ«іБөнЈ¬ВБАлЧУіБөнНкИ«ПыК§Ј®НЁ№эјЖЛг»ШҙрПВБРОКМвЈә
(1)ПЎБтЛбөДОпЦКөДБҝЕЁ¶ИОӘ______mol/L
(2)»мәПОпЦРВБөДЦКБҝОӘ______ЎЈ
(3)·ҙУҰәуИЬТәЦРјУИл4mol/L NaOHИЬТәөДМе»эЦБЙЩОӘ¶аЙЩәБЙэІЕДЬК№ЗвСх»ҜВБәНЗвСх»ҜГҫіБөн·ЦҝӘЈҝ______ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіҝОНв»о¶ҜРЎЧйЙијЖИзНјЛщКҫЧ°ЦГЦЖИЎҪП¶аБҝТТЛбТТхҘЎЈТСЦӘЈәўЩОЮЛ®ВИ»ҜёЖҝЙУлТТҙјРОіЙДСИЬУЪЛ®өДCaCl2ЎӨ6C2H5OHЎЈ
ўЪУР№ШУР»ъОпөД·РөгЈә
КФјБ | ТТГС | ТТҙј | ТТЛб | ТТЛбТТхҘ |
·РөгЈЁЎжЈ© | 34.7 | 78.5 | 118 | 77.1 |
ПВБРЛө·ЁХэИ·өДКЗ
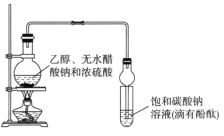
A.Ч°ЦГЦРЗтРО№ЬјИДЬАдДэХфЖшУЦДЬ·АЦ№ө№Оь
B.·ҙУҰҪбКшәуҙуКФ№ЬЦРөДПЦПуКЗЈәИЬТә·ЦІгЈ¬ПВІгОЮЙ«УНЧҙТәМеЈ»ЙПІгИЬТәСХЙ«ұдЗі
C.ҙУҙуКФ№ЬЦР·ЦАліцөДТТЛбТТхҘЦР»№ә¬УРТ»¶ЁБҝөДТТҙјЎўТТГСәНЛ®Ј¬УҰПИјУИлОЮЛ®ВИ»ҜёЖЈ¬№эВЛ·ЦАліцТТҙј
D.ЧоәујУИлОЮЛ®БтЛбДЖЈ¬И»әуҪшРРХфБуЈ¬КХјҜ118ЎжЧуУТөДБу·ЦЈ¬ТФөГөҪҪПҙҝҫ»өДТТЛбТТхҘЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝAЎўBЎўCЎўDКЗФӘЛШЦЬЖЪұнЦРЗ°36әЕФӘЛШЈ¬ЛьГЗөДәЛөзәЙКэТАҙОФцҙуЎЈөЪ¶юЦЬЖЪФӘЛШAФӯЧУөДәЛНвіЙ¶ФөзЧУКэКЗОҙіЙ¶ФөзЧУКэөД2ұ¶ЗТУР3ёцДЬј¶Ј¬BФӯЧУөДЧоНвІгp№мөАөДөзЧУОӘ°лідВъҪб№№Ј¬CКЗөШҝЗЦРә¬БҝЧо¶аөДФӘЛШЎЈDКЗөЪЛДЦЬЖЪФӘЛШЈ¬ЖдФӯЧУәЛНвЧоНвІгөзЧУКэУлЗвФӯЧУПаН¬Ј¬ЖдУаёчІгөзЧУҫщідВъЎЈЗл»ШҙрПВБРОКМвЈә
(1)AЎўBЎўCөДөЪТ»өзАлДЬУЙРЎөҪҙуөДЛіРтКЗ________(УГ¶ФУҰөДФӘЛШ·ыәЕұнКҫ)Ј»»щМ¬DФӯЧУөДјЫөзЧУЕЕІјКҪОӘ______________________ЎЈ
(2)AөДЧоёЯјЫСх»ҜОп·ЦЧУЦРЈ¬ЖдЦРРДФӯЧУІЙИЎ________ФУ»ҜЈ»BC3-өДБўМе№№РНОӘ________(УГОДЧЦГиКц)ЎЈ
(3)1 mol AB-ЦРә¬УРөДҰРјьёцКэОӘ________ЎЈ
(4)»ҜәПОпCH3COO[Cu(NH3)3ЎӨCO]ЦРУлCuЈ«РОіЙЕдАлЧУөДЕдМеОӘ____________(Мо»ҜС§КҪ)ЎЈ
(5) CH3COOHЦРCФӯЧУФУ»Ҝ№мөААаРНОӘ_________________ЎЈ
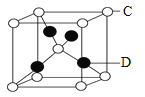
(6)ФӘЛШDУлФӘЛШCРОіЙТ»ЦЦ»ҜәПОпЖдҫ§°ыҪб№№ИзНјЛщКҫЈ¬ёГ»ҜәПОпөД»ҜС§КҪОӘ______.
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОТ№ъҝЖС§јТФЪМмИ»ЖшНСБтСРҫҝ·ҪГжИЎөГБЛРВҪшХ№Ј¬ЖдФӯАнИзНјЛщКҫЎЈПВБРУР№ШЛө·ЁҙнОуөДКЗЈЁ Ј©
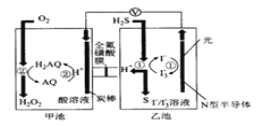
A.НјЦРөјПЯЙПұкјЗ·ҪПтОӘөзЧУБчПт
B.Ч°ЦГЦРH+ПтјЧіШЗЁТЖ
C.Хэј«ЙПөДөзј«·ҙУҰКҪОӘO2+4H++4eЈӯ=2H2O
D.ТТіШИЬТәЦР·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪЈәH2S+I3Јӯ =3IЈӯ+SЎэ+2H+
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com