
 合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起到重要作用.
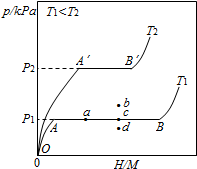
合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起到重要作用.分析 (1)zMHx(s)+H2(g)?zMHy(s)中遵循质量守恒定律,则反应前后H原子个数相同;吸氢速率v=$\frac{\frac{240mL}{2g}}{4min}$;由图可知,相同氢原子与金属原子的个数比时,T2温度高,对应的平衡时氢气的压强大,则升高温度,平衡逆向移动;
(2)T2温度高,对应的平衡时氢气的压强大,则升高温度,平衡逆向移动,则该反应为放热反应,低温下有利于吸收氢;当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,因温度不变,K不变,则平衡时氢原子与金属原子的个数比增大,平衡点在曲线AB上;释放氢气即为平衡逆向移动,结合该反应为放热反应、气体体积减小的反应特点解答;
(3)①CH4(g)+2H2O═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,由盖斯定律可知,②-①得到CO(g)+3H2(g)═CH4(g)+H2O(g),以此来解答.
解答 解:(1)zMHx(s)+H2(g)?zMHy(s)中遵循质量守恒定律,则反应前后H原子个数相同,则zx+2=zy,解得z=$\frac{2}{y-x}$;吸氢速率v=$\frac{\frac{240mL}{2g}}{4min}$=30mL•g-1•min-1;由图可知,相同氢原子与金属原子的个数比时,T2温度高,对应的平衡时氢气的压强大,则升高温度,平衡逆向移动,可知正反应△HⅠ<0,
故答案为:$\frac{2}{y-x}$;30;<;
(2)T2温度高,对应的平衡时氢气的压强大,则升高温度,平衡逆向移动,则该反应为放热反应,低温下有利于吸收氢,T1<T2时,则η(T1)>η(T2);当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,因温度不变,K不变,平衡时氢原子与金属原子的个数比增大,平衡点在曲线AB上,则达到平衡后反应(Ⅰ)可能处于图中的c点;释放氢气即为平衡逆向移动,因该反应为放热反应、气体体积减小的反应,则该贮氢合金可通过加热或减压的方式释放氢气,
故答案为:>;c;加热;减压;
(3)①CH4(g)+2H2O═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,由盖斯定律可知,②-①得到CO(g)+3H2(g)═CH4(g)+H2O(g),△H=-41kJ•mol-1-(+165kJ•mol-1)=-206kJ/mol,则热化学方程式为CO(g)+3H2(g)═CH4(g)+H2O(g)△H=-206kJ/mol,
故答案为:CO(g)+3H2(g)═CH4(g)+H2O(g)△H=-206kJ/mol.
点评 本题为2015年山东高考题30题,涉及化学平衡、热化学反应式、反应热计算及图象分析,把握平衡移动的影响因素、图象中纵横坐标的含义为解答的关键,(2)为解答的难点,侧重分析与应用能力的综合考查,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H20 | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
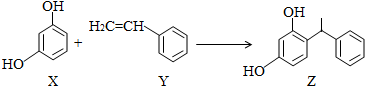
| A. | X、Y和Z均能使溴水褪色 | |
| B. | X和Z均能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
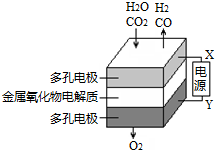 在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2e-═H2+O2-,CO2+2e-═CO+O2- | |
| C. | 总反应可表示为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Y | Z | ||
| X | W |
| A. | 原子半径:X<Y<Z | |
| B. | 气态氢化物的稳定性:X>Z | |
| C. | Z、W均可与Mg形成离子化合物 | |
| D. | 最高价氧化物对应水化物的酸性:Y>W |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2s22p3和2s22p4 | B. | 3s23p4和2s22p4 | C. | 3s2和2s22p3 | D. | 3s23p1和3s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中下图是己经合成的最著名的硫-氮化合物的分子结构.有关该物质说法错误的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中下图是己经合成的最著名的硫-氮化合物的分子结构.有关该物质说法错误的是( )| A. | 分子式为S4N4 | B. | 分子中既有极性键又有非极性键 | ||
| C. | 熔点低于同类晶体S2N2 | D. | 熔沸点低,硬度较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO、MgO、Na2O2均属于碱性氧化物 | B. | 盐酸、醋酸、苯酚均属于强电解质 | ||
| C. | CO2、CCl4、蛋白质均属于有机物 | D. | 液氯、晶体硅、臭氧均属于单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
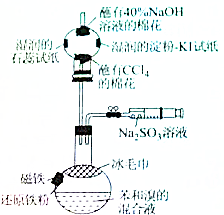 溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应,实验步骤如下:
溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应,实验步骤如下: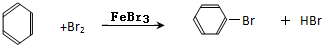 ;冰毛巾覆盖在圆底烧瓶上半部分的目的降低温度圆底烧瓶上部温度,起冷却回流作用;
;冰毛巾覆盖在圆底烧瓶上半部分的目的降低温度圆底烧瓶上部温度,起冷却回流作用;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com