
| T/”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
·ÖĪö £Ø1£©øł¾ŻĪĀ¶Č¶Ō»ÆŃ§Ę½ŗā”¢»ÆŃ§Ę½ŗā³£ŹżµÄÓ°ĻģĄ“»Ų“š£¬Ę½ŗā³£ŹżĖęĪĀ¶ČÉżøßŌö“ó£¬ĖµĆ÷Ę½ŗāÕżĻņ½ųŠŠ£»
£Ø2£©ÉżĪĀ”¢¼ÓŃ¹”¢Ōö¼ÓÅØ¶Č”¢Ź¹ÓĆ“ß»Æ¼ĮµČÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“ó£¬øł¾Ż»ÆŃ§Ę½ŗāŅʶÆŌĄķČ·¶ØĘ½ŗāµÄŅĘ¶Æ·½Ļņ£»
£Ø3£©»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾£ŗÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷×é·Öŗ¬Įæ±£³Ö²»±ä£¬¾Ż“Ė»Ų“š£»
£Ø4£©Ä³ĪĀ¶ČĻĀ£¬ø÷ĪļÖŹµÄĘ½ŗāÅØ¶Č·ūŗĻĻĀŹ½£ŗc£ØCO2£©£®c£ØH2£©=c£ØCO£©£®c£ØH2O£©£¬ĖµĆ÷ K=1£¬ÓÉ“Ė·ÖĪö½ā“š£»
£Ø5£©ŅĄ¾Ż»ÆŃ§Ę½ŗāČż¶ĪŹ½ĮŠŹ½ŗĶĘ½ŗā³£ŹżøÅÄī¼ĘĖćĻūŗÄĒāĘųĪļÖŹµÄĮæ¼ĘĖćµĆµ½Ę½ŗāדĢ¬ĻĀµÄĪļÖŹµÄĮ森
½ā“š ½ā£ŗ£Ø1£©»ÆŃ§Ę½ŗā³£ŹżµÄ“óŠ”Ö»ÓėĪĀ¶ČÓŠ¹Ų£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņĪüČȵķ½ĻņŅĘ¶Æ£¬ÓɱķæÉÖŖ£ŗÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗā³£ŹżŌö“ó£¬ĖµĆ÷»ÆŃ§Ę½ŗāÕżĻņŅĘ¶Æ£¬Ņņ“ĖÕż·“Ó¦·½ĻņĪüČČ£¬
¹Ź“š°øĪŖ£ŗĪüČČ£»
£Ø2£©a£®¼°Ź±·ÖĄė³öCOĘųĢ壬ÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ½µµĶ£¬¹Ź“ķĪó£»
b£®ŹŹµ±ÉżøßĪĀ¶Č£¬ÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¹ŹÕżČ·£»
c£®Ōö“óCO2µÄÅØ¶Č£¬ÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¹ŹÕżČ·£»
d£®Ń”Ōńøߊ§“߻ƼĮ£¬ÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“󣬵«ŹĒ²»ŅżĘšĘ½ŗāµÄŅĘ¶Æ£¬¹Ź“ķĪó£®
¹ŹŃ”bc£»
£Ø3£©a”¢·“Ó¦ŹĒŅ»øö·“Ó¦Ē°ŗóĢå»ż²»±äµÄ·“Ó¦£¬Ń¹ĒæµÄøı䲻»įŅŖŅżĘšĘ½ŗāŅĘ¶Æ£¬¹Ź“ķĪó£»
b”¢»ÆŃ§Ę½ŗāŹ±£¬ø÷×é·ÖµÄÅØ¶Č²»Ėꏱ¼äµÄøıä¶ųøı䣬¹ŹÕżČ·£»
c”¢»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒvÕż=vÄę£¬ĖłŅŌvÕż£ØH2£©=vÄę£ØH2O£©±ķĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹCÕżČ·£»
d”¢c£ØCO2£©=c£ØCO£©Ź±£¬²»ÄܱķĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬²»Ņ»¶Ø“ļµ½ĮĖĘ½ŗāדĢ¬£¬¹Ź“ķĪó£»
¹ŹŃ”bc£»
£Ø4£©Ä³ĪĀ¶ČĻĀ£¬ø÷ĪļÖŹµÄĘ½ŗāÅØ¶Č·ūŗĻĻĀŹ½£ŗc£ØCO2£©£®c£ØH2£©=c£ØCO£©£®c£ØH2O£©£¬ĖµĆ÷ K=1£¬¶ŌÓ¦µÄĪĀ¶ČŹĒ830”ę£¬¹Ź“š°øĪŖ£ŗ830£»
£Ø5£©ČōŌŚ£Ø3£©Ėł“¦µÄĪĀ¶ČĻĀ£¬ŌŚ1LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė2mol CO2ŗĶ3mol H2³ä·Ö·“Ó¦“ļĘ½ŗāŹ±£¬ÉčĒāĘųĻūŗÄĪļÖŹµÄĮæĪŖx£»
CO2£Øg£©+H2£Øg£©?CO£Øg£©+H2O£Øg£©
ĘšŹ¼Įæ£Ømol/L£© 2 3 0 0
±ä»ÆĮæ£Ømol/L£© x x x x
Ę½ŗāĮæ£Ømol/L£© 2-x 3-x x x
K=$\frac{{x}^{2}}{£Ø2-x£©•£Ø3-x£©}$=1£¬¼ĘĖćµĆµ½£ŗx=1.2£¬·“Ó¦“ļĘ½ŗāŹ±£¬H2µÄĪļÖŹµÄĮæ3mol-1.2mol=1.8mol£»CO2µÄĪļÖŹµÄĮæĪŖ0.8mol£¬
¹Ź“š°øĪŖ£ŗb£»c£®
µćĘĄ ±¾Ģāæ¼²éѧɜ¶ŌĘ½ŗā³£ŹżKµÄøıäÓėĘ½ŗāŅʶÆÖ®¼äµÄ¹ŲĻµµÄĄķ½ā£¬ŅŌ¼°Ó°Ļģ»ÆŃ§Ę½ŗāµÄŅņĖŲ£¬¼°ĄūÓĆĘ½ŗā³£ŹżK½ųŠŠ¼ņµ„µÄ¼ĘĖćÄÜĮ¦£¬ÄŃ¶Č²»“ó£®


 ĆūŠ£ĶØŠŠÖ¤ÓŠŠ§×÷ŅµĻµĮŠ“š°ø
ĆūŠ£ĶØŠŠÖ¤ÓŠŠ§×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ѧŠ£»Æѧъ¾æŠ”×é¶ŌijČÜŅŗ½ųŠŠ¼ģ²ā·ÖĪö£¬øĆĪŽÉ«ČÜŅŗÖŠæÉÄÜŗ¬ÓŠNH4+”¢K+”¢Al3+”¢HCO3-”¢Cl-”¢MnO4-”¢SO42-µČĄė×ÓÖŠµÄ¼øÖÖĄė×Ó£®
ѧŠ£»Æѧъ¾æŠ”×é¶ŌijČÜŅŗ½ųŠŠ¼ģ²ā·ÖĪö£¬øĆĪŽÉ«ČÜŅŗÖŠæÉÄÜŗ¬ÓŠNH4+”¢K+”¢Al3+”¢HCO3-”¢Cl-”¢MnO4-”¢SO42-µČĄė×ÓÖŠµÄ¼øÖÖĄė×Ó£® £¬æռ乹ŠĶĪŖČż½Ē׶ŠĪ£®
£¬æռ乹ŠĶĪŖČż½Ē׶ŠĪ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½µµĶĪĀ¶Č | B£® | ±£³ÖŃ¹Ēæ³äČėN2 | ||
| C£® | ±£³ÖĢå»ż²»±ä£¬Ōö¼ÓO2 | D£® | Ōö“óŃ¹Ēæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaÓėĖ®·“Ó¦£ŗNa+H2OØTNa++OH-+H2”ü | |
| B£® | Ļņ·ŠĖ®ÖŠµĪ¼Ó±„ŗĶFeCl3ČÜŅŗÖʱøFe£ØOH£©3½ŗĢå£ŗFe3++3H2O$\frac{\underline{\;V\;}}{\;}$Fe£ØOH£©3”ż+3H+ | |
| C£® | ŹµŃéŹŅŹ¢×°NaOHČÜŅŗµÄŹŌ¼ĮĘæ²»ÄÜÓĆ²£Į§Čū£ŗSiO2+2OH-ØTSiO32-+H2O | |
| D£® | ĻņĢ¼ĖįĒāøĘČÜŅŗÖŠ¼ÓČė¹żĮæµÄĒāŃõ»ÆÄĘČÜŅŗ£ŗCa2++OH-+HCO3-ØTCaCO3”ż+H2O+CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® | 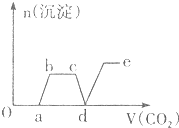 | ||
| C£® | 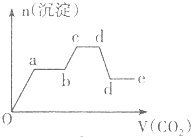 | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņH2SO4ČÜŅŗÖŠ¼ÓČėBa£ØOH£©2ČÜŅŗ | B£® | ĻņAlCl3ČÜŅŗÖŠĶØČė°±Ęų | ||
| C£® | ĻņNa2SČÜŅŗÖŠĶØČėSO2 | D£® | ĻņFe2£ØSO4£©3ČÜŅŗÖŠ¼ÓČėCu |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| CaCO3 | CaSO4 | Mg£ØOH£©2 | MgCO3 |
| 1.4”Į10-3 | 2.55”Į10-2 | 9”Į10-4 | 1.1”Į10-2 |
| A£® | ĮņĖįøĘŠü×ĒŅŗÖŠ“ęŌŚCaSO4£Øs£©?Ca2+£Øaq£©+SO42-£Øaq£© | |
| B£® | ÓĆNa2CO3ČÜŅŗ½žÅŻ¹ųĀÆÖŠµÄĖ®¹ø£¬æɽ«Ė®¹øÖŠµÄCaSO4×Ŗ»ÆĪŖCaCO3 | |
| C£® | ĻņMg£ØOH£©2Šü×ĒŅŗÖŠµĪ¼ÓFeCl3£¬³Įµķ±äĪŖŗģŗÖÉ«£¬ĖµĆ÷Čܽā¶ČFe£ØOH£©3£¼Mg£ØOH£©2 | |
| D£® | Ļņ2ml±„ŗĶMgCl2 ČÜŅŗÖŠĻČŗóµĪ¼Ó0.1mol/LµÄNa2CO3”¢NaOHČÜŅŗø÷2µĪ£¬²śÉśµÄ°×É«³ĮµķĪŖMg£ØOH£©2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com