
| A. | pH=n | B. | pH=-lg n | C. | pH=14-lgn | D. | pH=lgn+14 |
分析 常温下用惰性电极电解1L含足量KCl的溶液,发生电极反应为:阳极:2Cl--2e-=Cl2↑,阴极:2H2O+2e-=H2↑+2OH-,结合反应可计算出电解后的溶液中的氢氧根离子浓度,再结合水的离子积计算出溶液中氢离子浓度,最后计算出溶液的pH.
解答 解:电解过程的电极反应式为:阳极:2Cl--2e-=Cl2↑,阴极:2H2O+2e-=H2↑+2OH-,
生成的氢氧根离子与转移的电子的物质的量相等,则通过n mol电子的电量时生成了nmol氢氧根离子,
电解后得到溶液的氢氧根离子浓度为nmol/L
则c(H+)=$\frac{1{0}^{-14}}{n}$,所以溶液的pH=-lg$\frac{1{0}^{-14}}{n}$,=lgn+14,
故选D.
点评 本题考查了溶液pH的计算,题目难度中等,根据电极反应式找出转移电子与氢氧根离子的物质的量关系为解答关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | SF6中的空间构型为正四面体形 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
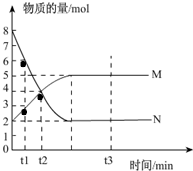 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,负极反应式:Cu2++2e-=Cu | |
| B. | 氯碱工业和电解精炼铜中,阳极都是氯离子放电放出氯气 | |
| C. | 在氯碱工业中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 | |
| D. | 电解精炼铜时,应用粗铜作阳极、精铜作阴极,可溶性铜盐作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
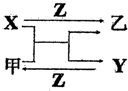 X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是( )
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是( )| A. | X、Y、Z一定都是非金属单质 | B. | X、Y、Z一定都是金属单质 | ||
| C. | X、Y、Z中至少有一种是非金属单质 | D. | X、Y、Z中至少有一种是金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO用于冶炼金属镁 | B. | NaCl用于制纯碱 | ||
| C. | Cu(OH)2用于检验糖尿病 | D. | FeCl3用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取、过滤、蒸馏、蒸馏 | B. | 过滤、分液、蒸馏、萃取 | ||
| C. | 过滤、蒸馏、过滤、蒸馏 | D. | 过滤、分液、过滤、蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com