
【题目】铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下: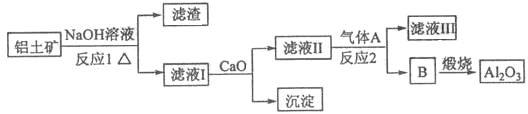
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下: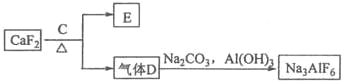
回答下列问题:
(1)写出反应1的化学方程式___________________________ ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为_______________ ;
(3)E可作为建筑材料,化合物C是_____ ,写出由D制备冰晶石的化学方程式 ____________;
(4)电解制铝的化学方程式是 _____________________________________,以石墨为电极,阳极产生的混合气体的成分是 _________________。
【答案】
(1)2NaOH+SiO2=Na2SiO3+H2O、2NaOH+Al2O3=2NaAlO2+H2O;
(2)CaSiO3;2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(3)浓H2SO4;12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O;
(4)2Al2O3(熔融)![]() 4Al+3O2↑;O2、CO2(或CO)
4Al+3O2↑;O2、CO2(或CO)
【解析】
试题分析:(1)铝土矿中能与氢氧化钠溶液反应的是氧化铝和二氧化硅,反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O、2NaOH+Al2O3=2NaAlO2+H2O;
(2)氧化钙溶于水生成氢氧化钙,氢氧化钙与硅酸钠反应生成硅酸钙沉淀;B煅烧得到氧化铝,说明B是氢氧化铝,能与偏铝酸钠反应生成氢氧化铝的气体是二氧化碳,反应的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(3)氟化钙与浓硫酸反应生成硫酸钙和HF,其中硫酸钙可以作为建筑材料。HF与碳酸钠、氢氧化铝反应生成冰晶石,根据原子守恒可知还有二氧化碳和水生成,则制备冰晶石的化学方程式为12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O;
(4)电解制铝的化学方程式是2Al2O3(熔融)![]() 4Al+3O2↑;以石墨为电极,阳极产生氧气,产生的氧气能与电极石墨在高温下反应生成CO或CO2,所以混合气体的成分是O2、CO2(或CO)。
4Al+3O2↑;以石墨为电极,阳极产生氧气,产生的氧气能与电极石墨在高温下反应生成CO或CO2,所以混合气体的成分是O2、CO2(或CO)。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构现进行如下实验:
①相同条件下,测得A的蒸气密度是H2密度的60倍
②6gA在一定条件下完全燃烧,生成3.36L二氧化碳(标况)和1.8g水
③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,等量的A能与足量的金属钠反应放出33.6L氢气(标况)试计算确定: (写过程)
(1)A的分子式____________________
(2)A的结构简式________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同系物的说法错误的是
①![]() 和
和![]() 互为同系物,均可以与金属钠反应。
互为同系物,均可以与金属钠反应。
②苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色。
③同系物在水中的溶解性相同,苯的同系物都难溶于水,乙醇的同系物都易溶于水。
④烷烃的密度随分子量增大而增大,液态烷烃的密度小于水的密度,固态烷烃的密度大于水的密度。
⑤同系物的分子式可以用一个通式概括,符合通式CnH2nO的物质是饱和一元醛。
⑥乙二醇和丙三醇互为同系物。
A.③④⑤⑥ B.①②③④ C.①②⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯G是一种用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,它的分子式为C10H10O2,用芳香烃A为原料合成肉桂酸甲酯G的路线如下:

已知:
(1)B的官能团的名称________。
(2)D→F的反应类型是________。
(3)肉桂酸甲酯的结构简式为_________。
(4)写出A的结构简式___________。
(5)C与银氨溶液反应的化学方程式________。
(6)D转化为E的化学方程式_________。
(7)写出符合下列条件的D的同分异构体的结构简式_______。
①苯环上有两个取代基且苯环上的一氯代物有两种;
②遇FeCl3溶液显紫色
③在NaOH溶液中反应最多能消耗3mol NaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届厦门一模】磷化氢( PH3)是一种剧毒气体,是最常用的高效熏蒸杀虫剂,也是一种电子工业原料。
(1)在密闭粮仓放置的磷化铝(AlP)片剂,遇水蒸气放出PH3气体,该反应的化学方程式为 。
(2)利用反应PH3+3HgCl2= P(HgCl)3 +3HCl,可准确测定微量的PH3。
①HgCl2溶液几乎不导电,说明HgCl2属于________________(填“共价”或“离子”)化合物。
②通过测定溶液____________变化,可测定一定体积空气中PH3的浓度。
(3)PH3的一种工业制法涉及的物质转化关系如下图所示: 
①亚磷酸属于________________元酸。
②当反应I生成的n(NaH2PO2):n(Na2HPO3) =3:1时,参加反应的n(P4):n(NaOH)= 。
(4)一种用于处理PH3废气的吸收剂成分为次氯酸钙80%、锯木屑(疏松剂)15%、活性炭2.5%、滑石粉(防结块)2.5%。
①次氯酸钙将PH3氧化为H3PO4的化学方程式为________________。
②空气中的水蒸气可加快PH3的氧化过程,其原因可能是____________。
(5)从(4)中的吸收残留物中回收磷酸氢钙(CaHPO4)的方法如下:
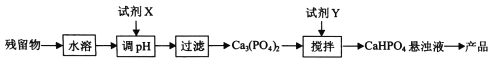
①试剂x为 (填化学式)。
②已知25℃时,H3PO4的Kal=7.5×10-3、Ka2=6.3×10-8、Ka3 =4.4×10-13。加入Y时,应控制悬浊液pH 7(填“>”、“=”或“<”),通过计算说明理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,物质①4gH2,②33.6LCH4,③1molH2O,④3.01×1023个O2。含分子数最多的是(填序号,下同) ,含原子数最少的是 ,质量最大的是 ,体积最小的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同分异构体的说法正确的是( )
A.乙烷的二氯代物和甲烷的二氯代物数目相同
B.丙烷的一氯代物有3种
C.苯的四氯代物有3种
D.C5H12的同分异构体有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)按要求完成下列反应的化学方程式
①1,3-丁二烯与溴单质能发生的两种加成反应 ,
②苯与浓硝酸、浓硫酸的混合物在60℃时的反应
③工业上,乙苯的制取反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届北京西城一模】Cu2O可用于制作船底防污漆,某学习小组探究制备Cu2O的方法。
【查阅资料】
① CuSO4与Na2SO3溶液混合可制备Cu2O。
② Cu2O为砖红色固体;酸性条件下生成Cu2+和Cu。
③ Cu2O和Cu(SO3)23-可以相互转化 ![]()
(1)配制0.25 mol·L-1CuSO4溶液和0.25 mol·L-1 Na2SO3溶液。测得CuSO4溶液pH=4,Na2SO3溶液
pH=9。用离子方程式表示CuSO4溶液pH=4的原因_______。
(2)完成CuSO4溶液和Na2SO3溶液反应制Cu2O的离子方程式:
![]()
【实验探究】
操作 | 现象 |
| i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5 mL时,溶液的蓝色消失。 ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生。 iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10 mL时,沉淀完全溶解,得无色溶液。 |
(3)证明ii中砖红色沉淀是Cu2O的实验方案是_________________。
(4)经检验i中黄色沉淀含有Cu2SO3,ii中沉淀由黄色变砖红色的化学方程式是________________。
(5)iii中砖红色沉淀消失的原因是_________________。
(6)在加热条件下,若向2 mL 0.25 mol·L-1Na2SO3溶液中滴加0.25 mol·L-1CuSO4溶液至过量,预期观察到的现象是_________________。
(7)由上述实验得出结论:CuSO4溶液和Na2SO3溶液反应制备Cu2O,应控制的条件是_______、_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com