
| A. | 常温下,反应C(s)+H2O(g)═CO(g)+H2(g)不能自发进行,则该反应的△H>0 | |
| B. | 一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H>0,△S<0 | |
| C. | 放热的自发过程,一定是熵增加的过程 | |
| D. | 液态水可自发挥发成水蒸气的过程是熵减的过程 |
分析 A、△H-T△S>0反应非自发进行,反应△S>0,△H>0;
B、气体的物质的量增加,所以△S>0;
C、△H-T△S<0反应自发进行;
D、态水变为气态水、扑克牌洗牌等都属于混乱(或无序)程度变大的过程.
解答 解:A、△H-T△S>0,反应非自发进行,反应△S>0,满足△H-T△S>0,则△H>0,故A正确;
B、气体的物质的量增加,所以△S>0,故B错误;
C、△H-T△S<0反应自发进行,所以熵不一定增加,故C错误;
D、液态水可自发挥发成水蒸气的过程,属于熵增的过程,故D错误;
故选A.
点评 本题考查学生影响化学反应方向的因素是:焓变和熵变,注意化学反应能否自发进行的判据是看△H-T△S是否小于零,必须综合考虑体系的焓变和熵变.


科目:高中化学 来源: 题型:解答题
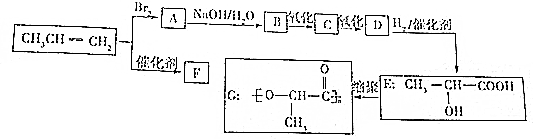
 .
.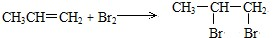 ,反应类型:加成反应;
,反应类型:加成反应;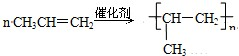 ,反应类型:加聚反应.
,反应类型:加聚反应.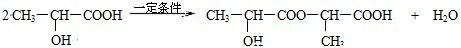 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在一定温度下,把2mol N2和6mol H2通入一个体积不变的密闭容器 中(如右图)发生以下的反应:
在一定温度下,把2mol N2和6mol H2通入一个体积不变的密闭容器 中(如右图)发生以下的反应:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
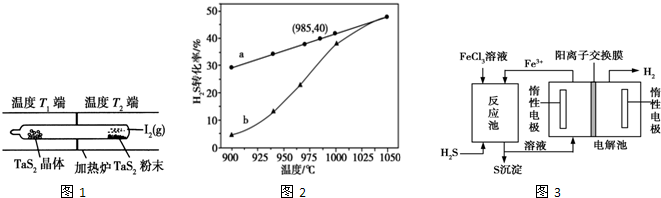
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+H2O?H2CO3 | B. | OH-+HS-?S2-+H2O | ||
| C. | HS-+H2O?H3O++S2- | D. | S2-+H2?HS-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.完成下列空白:
A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.完成下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图装置用于分离沸点相关较大的互溶液体混合物 | |
| B. | 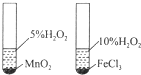 如图装置用于研究不同催化剂对反应速率的影响 | |
| C. | 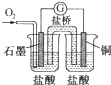 图中电流计的指针发生偏转,石墨为正极 | |
| D. |  如图装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com