
分析 由结构简式可知,分子中含碳碳双键、-CHO,均能被强氧化剂氧化,应先利用弱氧化剂检验-CHO,结合烯烃、醛的性质来解答.
解答 解:(1)检验分子中醛基的常用试剂是银氨溶液或新制的氢氧化铜;反应现象为产生银镜反应或产生红色沉淀,化学方程式为(CH3)2C=CHCHO+2Ag(NH3)2OH$→_{△}^{水浴}$(CH3)2C=CHCOONH4+2Ag↓+3NH3+H2O或(CH3)2C=CHCHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C=CHCOOH+Cu2O+H2O,
故答案为:银氨溶液或新制的氢氧化铜;产生银镜反应或产生红色沉淀;(CH3)2C=CHCHO+2Ag(NH3)2OH$→_{△}^{水浴}$(CH3)2C=CHCOONH4+2Ag↓+3NH3+H2O或(CH3)2C=CHCHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C=CHCOOH+Cu2O+H2O;
(2)检验该分子中碳碳双键的方法是将银镜反应(上述反应)后的溶液调节至中性,加溴水,观察是否褪色,
故答案为:将银镜反应(上述反应)后的溶液调节至中性,加溴水,观察是否褪色;
(3)碳碳双键、-CHO,均能被强氧化剂氧化,应先利用弱氧化剂检验-CHO,则实际操作中,哪一个官能团应先检验醛基(或-CHO),
故答案为:醛基(或-CHO).
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意烯烃及醛的性质,题目难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:实验题
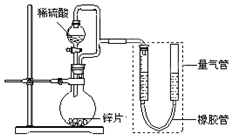 某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.| 序号 | V(H2SO4)/mL | c(H2SO4)/mol•L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与Fe粉完全反应时转移电子数为2NA | |
| B. | 过氧化钠与水反应时,每生成1molO2,转移4mol电子 | |
| C. | 标准状况下,11.2L氟化氢中含有氟原子的数目为0.5NA | |
| D. | 0.1 mol•L-1NaHSO4溶液中,阳离子数目之和为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和丙烯 | B. | 乙烷和2-丁烯 | ||
| C. | 甲烷和2-甲基丙烯 | D. | 乙烯和1-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
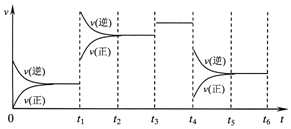 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )| A. | t1时升高了温度 | B. | t3时加入了催化剂 | ||
| C. | t5~t6时刻,Y转化率最小 | D. | 在t3~t4时间内,X的体积分数最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液中通入CO2: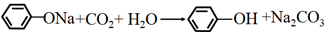 | |
| B. | 常温下CH2=CHCH3与水接触:CH2=CHCH3+H2O→CH3CH(OH)CH3 | |
| C. | 乙醇和金属钠发生反应放出氢气:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑ | |
| D. | 甲苯与氯气在铁粉催化作用下发生反应: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用玻璃棒蘸取NaClO溶液点在干燥的PH试纸上,试纸呈现蓝色,证明HClO是弱酸 | |
| B. | 将一定量的FeCl3晶体、盐酸依次加入容量瓶中,配制一定物质的量浓度的FeCl3溶液 | |
| C. | 为证明Cu与浓硫酸反应生成了CuSO4,可将反应后的混合液冷却后再加入水,若显色即可证明生成了CuSO4 | |
| D. | 用乙醇、乙酸及浓硫酸制取乙酸乙酯的过程中发现忘加碎瓷片,需在完全冷却后再补 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com