
A、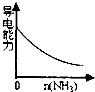 氨气通入硫酸溶液中 |
B、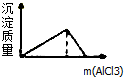 NaOH溶液中逐滴加入AlCl3溶液至过量 |
C、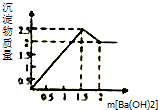 向1L1.0mol?L-1的明矾溶液中加入Ba(OH)2溶液 |
D、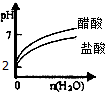 pH=2的盐酸和醋酸分别加水稀释 |


科目:高中化学 来源: 题型:
| A、用10mL量筒量取8.16mL稀盐酸 |
| B、用托盘天平称取25.20gNaCl |
| C、用广泛pH试纸测得某溶液的pH为2.3 |
| D、用25mL碱式滴定管进行中和滴定时,用去某浓度的碱溶液21.70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的pH增大 |
| B、CH3COOH的电离程度变大 |
| C、溶液的导电能力减弱 |
| D、溶液中c(OH-)减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M的相对原子质量为32 |
| B、电解过程中溶液的pH不发生变化 |
| C、M的相对原子质量为64 |
| D、电路中通过0.5mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有AgCl沉淀 |
| B、只有AgI沉淀 |
| C、AgCl、AgI都沉淀都有 |
| D、没法确定是那种沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O+H2O?H3O++OH- |
| B、CO32-+H2O?HCO3-+OH- |
| C、NH3+H2O?NH3.H2O |
| D、HCO3-+OH-?H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸镁 | B、青霉素 |
| C、阿司匹林 | D、麻黄碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com