
【题目】常温下,用0.10 mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1 CH3COONa溶液和NaCN溶液,所得滴定曲线如右图(忽略体积变化)。下列说法正确的是

A. 溶液中阳离子的物质的量浓度之和:点②等于点③
B. 点①所示溶液中:c(CN—)+ c(HCN)=2c(Cl—)
C. 点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)> c(CH3COOH)
D. 点④所示溶液中:c(Na+)+ c(CH3COOH)+ c(H+)>0.10 mol·L-1
【答案】BD
【解析】A.根据电荷守恒,点②中存在c(CH3COO-)+ c(OH-)+ c(Cl—)= c(Na+)+ c(H+),点③中存在c(CN—)+ c(OH-)= c(Na+)+ c(H+),由于两点的溶液体积不等,溶液的pH相等,则c(Na+)不等,c(H+)分别相等,因此阳离子的物质的量浓度之和不等,故A错误;B. 点①所示溶液中含有等物质的量浓度的NaCN、HCN和NaCl,存在物料守恒,c(CN—)+ c(HCN)=2c(Cl—),故B正确;C. 点②所示溶液中含有CH3COONa、CH3COOH和NaCl,其中CH3COONa的浓度略大于CH3COOH和NaCl,溶液的pH=5,说明乙醋酸的电离为主,因此c(CH3COO-)> c(Cl-),故C错误;D. 点④所示溶液为等物质的量浓度的醋酸和氯化钠,浓度均为0.05 mol·L-1,则c(Na+)= c(Cl-)=0.05 mol·L-1,c(CH3COO-)+ c(CH3COOH)=0.05 mol·L-1,根据电荷守恒,c(CH3COO-)+ c(OH-)+ c(Cl—)= c(Na+)+ c(H+),因此c(CH3COO-)= c(H+)- c(OH-),则c(Na+)+ c(CH3COOH)+ c(H+)=0.05 mol·L-1+0.05 mol·L-1-c(CH3COO-)+ c(H+)=0.10 mol·L-1- c(H+)+ c(OH-)+ c(H+)=0.10 mol·L-1+ c(OH-)>0.10 mol·L-1,故D正确;故选BD。


科目:高中化学 来源: 题型:
【题目】早在西汉时期就有记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱,要加快该化学反应的速率,所采取的下列措施无效的是( )
A.增大硫酸铜的浓度B.提高反应的温度
C.增大压强D.用铁粉代替铁片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。请回答下列问题:
(1)若将饱和氯化铁溶液分别滴入下列物质中,能形成胶体的是______________(填字母,下同)。
A.冷水 B.沸水 C.氢氧化钠浓溶液 D.氯化钠浓溶液
(2)甲、乙、丙三名同学进行氢氧化铁胶体的制备操作如下,其正确的是____________。
A.甲同学取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL 氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热
B.乙同学直接加热饱和氯化铁溶液
C.丙同学向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟
(3)写出制备氢氧化铁胶体的化学方程式________________________________。
(4)证明有氢氧化铁胶体生成的实验操作是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的联接并填空:
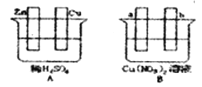
(1)在A图中,使铜片上冒H2气泡。请加以必要联接①______(在答题卡的图中画线),则联接后的装置叫②______。电极反应式:锌板:③_______;铜板:④_______。
(2)在B图中(a、b均为惰性电极),使a极析出铜,则b析出①______。加以必要的联接后,该装置叫②_____。电极反应式:a极:③_______b极:④___________。经过一段时间后,停止反应并搅均溶液,溶液的pH值⑤______(升高、降低、不变),加入一定量的⑥_____后,溶液能恢复至与电解前完全一致。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解池应用的规律提炼题组某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
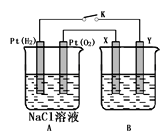
(1)通O2的Pt电极为电池__________极(填电极名称),其电极反应式为______________。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为_________,电解质溶液为__________。
(3)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,在__________电极(填“X”或“Y”)周围有固体沉积成阳极泥,阳极泥的成分为___________。
(4)若X、Y均为Pt,B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全逸出,溶液体积不变)。恢复到常温下,B电池溶液的pH=___________,要使该溶液恢复到原来的状态,需加入__________(填物质并注明物质的量)。
(5)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为_______________。
(学法题)通过以上题目,请总结书写电极反应式的关键____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氢键,下列说法正确的是( )
A. 含氢元素的化合物中一定有氢键
B. 氢键比分子间作用力强,所以它属于化学键
C. DNA中的碱基互补配对是通过氢键来实现的
D. H2O是一种非常稳定的化合物,这是由于氢键所致
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com