
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是 ( )
A. 同周期元素中X的金属性最强
B. 原子半径X>Y,离子半径X+>Z2-
C. 同族元素中Z的氢化物稳定性最高
D. 同周期元素中Y的最高价含氧酸的酸性最强
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
五种短周期元素的某些性质如下表所示,其中W、Y、Z为同周期元素,下列说法正确的是
元素代号 | X | W | Y | Z | Q |
原子半径(×10-12m) | 37 | 64 | 66 | 70 | 154 |
主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
A.Z与X之间形成的化合物具有还原性
B.由Q与Y形成的化合物中只存在离子键
C.由X、Y、Z三种元素形成的化合物的水溶液呈碱性
D.Y与W形成的化合物中,Y显负价
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下期末化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.标准状况下,1 L庚烷所含有的分子数为NA/22.4
B.1 mol甲基(—CH3)所含电子数为9NA
C.标准状况下,B2H6和C2H4的混合气体22.4 L,所含的电子数约为16NA
D.26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
将一定质量铜与100 mL一定浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液加入140mL 5 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀,则原硝酸溶液的物质的量浓度是( )
A.5 mol/L B.7 mol/L C.10mol/L D.12 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
可逆反应: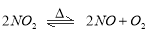 在固定容积的密闭容器中反应,达到平衡状态的标志是( )
在固定容积的密闭容器中反应,达到平衡状态的标志是( )
(1)单位时间内生成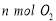 的同时生成
的同时生成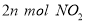
(2)单位时间内生成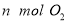 的同时生成
的同时生成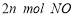
(3)用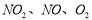 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
的物质的量浓度变化表示的反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
A.(1)(4) B.(2)(3) C.(1)(3)(4) D.(1)(2)(3)(4)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
我国稀土资源丰富。下列有关稀土元素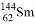 与
与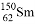 的说法正确的是 ( )
的说法正确的是 ( )
A. 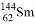 与
与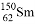 互为同位素
互为同位素
B. 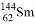 与
与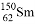 的质量数相同
的质量数相同
C. 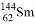 与
与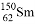 是同一种核素
是同一种核素
D. 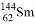 与
与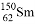 的核外电子数和中子数均为62
的核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高二下期末化学试卷(解析版) 题型:选择题
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为
A.0.15 mol·L-1
B.0.2 mol·L-1
C.0.3 mol·L-1
D.0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
现有如下溶液:
①1.0mL0.10mol•L-1双氧水
②1.0mL0.20mol•L-1双氧水
③3.0mL0.10mol•L-1KMnO4溶液
④3.0mL0.010mol•L-1KMnO4溶液。
所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢:
(1)写出发生反应的离子方程式_________________________;若某反应的化学方程式为2KMnO4+9H2O2+3H2SO4=K2SO4+2MnSO4+7O2↑+12H2O,则该反应的氧化剂为______________,若有9molH2O2参加该反应,则反应转移电子数目为___________;
(2)某温度下,若要探究反应物浓度对反应速率的影响,则应选择试剂______进行实验(填序号)。
(3)某温度下,某同学按照(2)中选择试剂进行实验,褪色时间为5s:
①计算以H2O2表示的反应速率为___________;
②进行实验过程中,该同学发现颜色变化会出现先慢后快并突然褪色的现象。为此该同学又进行了一次平行实验,只是加入少量MnSO4固体,结果溶液立即褪色,请推测颜色变化会出现先慢后快并突然褪色的现象的原因___________;
(4)某同学在不同温度下,分别取两份等体积不同浓度的双氧水与等量KMnO4溶液进行反应,绘制出c(H2O2)随时间(t)变化的曲线如图所示,若A、B分别为不同温度时测定的曲线,则_____(填“A”或“B”)曲线所对应的实验温度高,判断的依据是___________;
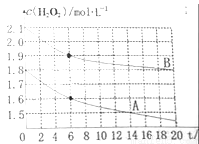
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一下期末化学试卷(解析版) 题型:选择题
反应2A(g)  2B(g)+E(g) △H>0 ,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
2B(g)+E(g) △H>0 ,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
A.加压 B.减压 C.减少E的浓度 D.降温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com