
【题目】根据题中信息完成下列填空题
(1)黄绿色气体单质X,与标况下密度为1.25g/L的烯烃Y发生加成反应,请写出烯烃Y的结构式__________。写出该加成产物的所有同分异构体结构简式______________。
(2)125℃,101kPa的条件下,某气态烯烃在氧气中充分燃烧后,气体体积没有变化,求出该烯烃的分子式________。
(3)某元素X的一种核素质量数为A,含N个中子,它与1H原子组成HmX分子。在a g HmX中所含质子的物质的量是___________mol。
(4)E和F均含有18个电子的微粒,E是所有18电子微粒中氧化能力最强的分子,请你写出E与水发生的化学反应方程式_______________。F是有两种元素组成的三原子分子,将其通入足量的NaOH溶液,发生的离子方程式_______________。
【答案】![]() CHCl2CH3 C2H4
CHCl2CH3 C2H4 ![]() F2+2H2O=4HF+O2 H2S+2OH-=S2-+2H2O
F2+2H2O=4HF+O2 H2S+2OH-=S2-+2H2O
【解析】
(1)黄绿色气体单质X是氯气,密度为1.25g/L的烯烃Y的相对分子质量是1.25×22.4=28,Y是乙烯,结构式为![]() ;氯气与乙烯发生加成反应得到1,2-二氯乙烷,则该加成产物的所有同分异构体结构简式为CHCl2CH3。
;氯气与乙烯发生加成反应得到1,2-二氯乙烷,则该加成产物的所有同分异构体结构简式为CHCl2CH3。
(2)125℃,101kPa的条件下,某气态烯烃在氧气中充分燃烧后,气体体积没有变化,根据燃烧通式CxHy+(x+![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O可知1+x+
H2O可知1+x+![]() =x+
=x+![]() ,解得y=4,则该烯烃的分子式为C2H4。
,解得y=4,则该烯烃的分子式为C2H4。
(3)某元素X的一种核素质量数为A,含N个中子,则质子数为A-N;它与1H原子组成HmX分子中质子数为,m+A-N,则在a g HmX中所含质子的物质的量是![]() mol。
mol。
(4)E和F均含有18个电子的微粒,E是所有18电子微粒中氧化能力最强的分子,E是F2,则E与水发生的化学反应方程式为F2+2H2O=4HF+O2。F是有两种元素组成的三原子分子,F是H2S,将其通入足量的NaOH溶液,发生的离子方程式为H2S+2OH-=S2-+2H2O。


科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是
A. 乙烯在空气中燃烧 B. 在镍做催化剂的条件下,苯与氢气反应
C. 在FeBr3催化作用下,苯与液溴反应 D. 乙醇在铜或银作催化剂条件下与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下:
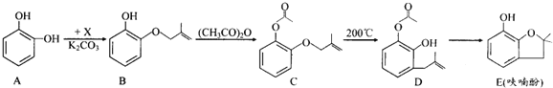
(1)A在空气中久置会由无色转变为棕褐色,其原因是____________,A在核磁共振氢谱中有___________组峰。
(2)B→C的反应类型是_____________________。
(3)已知X的分子式为C4H7Cl。写出A→B的化学方程式:___________________。
(4)要鉴别化合物C和D,适宜的试剂是__________________________。
(5)B的同分异构体很多,符合下列条件的有______种,写出其中能发生银镜反应的同分异构体的结构简式:__________(任写一种)。
①苯的衍生物 ②有两个互为对位的取代基 ③含有酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图-1和图-2所示。
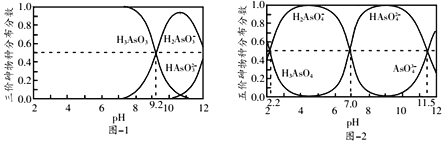
下列说法错误的是( )
A. H3AsO3和Na2HAsO4水溶液可以发生复分解反应
B. H3AsO4水溶液中存在:![]()
C. 向 H3AsO4的溶液中加入一定量的NaOH溶液至pH=5时,![]()
D. 室温下向含0.2mol H3AsO4的溶液中加入12gNaOH固体,所得溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及主要化合价如下表
元素代号 | X | Y | Z | M | R | w |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 | 0.077 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 | +4 -4 |
已知:X是短周期中最活泼的金属,且与R同周期。请用相应的化学用语或者化学符号回答下列问题。
(1)R在元素周期表中的位置为________________。
(2)X与M按原子个数比1:1构成的物质的电子式为_____________;所含化学键类型___________。
(3)X+、Y2-、M2-、R3+离子半径大小顺序为__________________________(用离子符号表示)。
(4)请用电子式表示WY2的形成过程___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________。
(2)利用甲醇燃料电池设计如下图所示的装置:则该装置中b极的电极反应式为_________________________; Zn极为_______极。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1~20号元素中A、B、C、D四种元素的原子中,质子数为A<B<C<D,A元素的原子最外层电子数是次外层电子数的2倍;B元素的原子核外M层电子数是L层电子数的一半;C元素的原子次外层电子数比最外层电子数多1个;D元素的原子核外K层。L层电子数之和等于M、N层电子数之和。试推断:
(1)元素B的原子结构示意图_______。
(2)C、D形成的化合物的电子式______。
(3)工业上由A元素的单质制取B元素的单质的化学方程式为____
(4)若没有“质子数为A<B<C<D”的限制,C还可以是____元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用一种微生物将废水中的有机物(如淀粉)和废气NO的化学能直接转化为电能,下列说法中一定正确的是
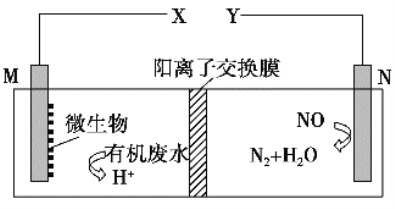
A. 质子透过阳离子交换膜由右向左移动
B. 与X相连接是用电器标有“+”的接线柱
C. M电极反应式:(C6H10O5)n+7nH2O-24ne-===6nCO2↑+24nH+
D. 当M电极微生物将废水中16.2 g淀粉转化掉时,N电极产生134.4 L N2(标况下)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com