
| A. | 氯碱工业 | B. | 高炉炼铁 | C. | 粗硅提纯 | D. | 硫酸工业 |
科目:高中化学 来源: 题型:选择题
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 氧化铜和氧化亚铜都是黑色固体 | |
| C. | 铝在高温下能还原锰、铁、铬等金属氧化物得到金属 | |
| D. | 因为镁和铝在空气中都能形成氧化膜,所以镁铝都不能溶于浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
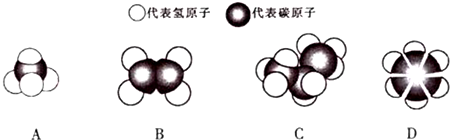
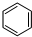 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$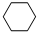 .
. .
.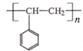 路线流程图(无机试剂任选).合成路线流程图示例如下:
路线流程图(无机试剂任选).合成路线流程图示例如下: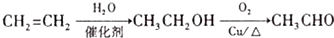
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
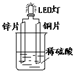
| A. | 锌片换成铁片,电路中的电流方向不变 | |
| B. | 铜电极的电极反应式为Cu2++2e-=Cu | |
| C. | 将硫酸换成柠檬汁,导线中仍有电子流动 | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
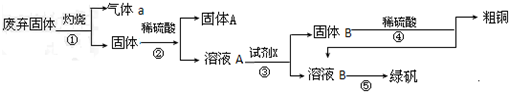
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
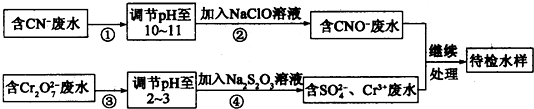
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的铁粉投入一定量的热浓硫酸中,将产生的气体通人浓NaOH溶液中,气体可全部被吸收 | |
| B. | 25℃下,pH=0的溶液中,A13+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$、Fe2+可以大量共存 | |
| C. | 检验红砖中的氧化铁,向红砖粉末中加人盐酸,充分反应后取上层清液于试管中,滴加2~3滴KSCN溶液即可 | |
| D. | 向CuSO4溶液中滴人过量NaOH溶液充分反应后,将混合溶液倒人蒸发皿中加热煮沸一段时间,然后冷却、过滤、滤纸上的物体为“蓝色固体” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 建筑使用了大量钢材,钢材是纯铁 | |
| B. | 明矾与水反应生成氢氧化铝胶体能吸附水中悬浮物,可用于水的净化 | |
| C. | Al2O3的熔点很高,可用于制作耐高温材料 | |
| D. | 用焰色反应可鉴别K2CO3和NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com