
|
下列物质中不能与CO2反应的是 | |
A. |
Na2O2固体 |
B. |
Na2CO3溶液 |
C. |
NaHCO3溶液 |
D. |
BaCl2溶液 |
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:阅读理解
(1)汽车排放的尾气中因含有氮的氧化物而污染大气,产生氮氧化物的主要原因是( )
A.燃烧含氮化合物燃料引起的 B.燃烧含铅汽油引起的
C.是由于燃烧不充分引起的 D.是在汽缸中N2被氧化生成的
(2)下列有关城市各项污染源与其造成的恶果排列正确的是( )
A.汽车尾气—光化学烟雾 工业废气—酸雨工业废水—“公害病”
B.汽车尾气—酸雨 工业废气—“公害病” 工业废水—光化学烟雾
C.汽车尾气—“公害病” 工业废气—酸雨 工业废水—光化学烟雾
D.汽车尾气—光化学烟雾 工业废气—“公害病” 工业废水—酸雨
(3)一氧化氮和一氧化碳都是汽车尾气里的有害物质,它们能缓慢地发生如下反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g);ΔH<0
N2(g)+2CO2(g);ΔH<0
现利用此反应,拟设计一种环保装置以消除汽车尾气对大气的污染。下列设计方案可以提高尾气处理效果的是( )
①选用适当的催化剂 ②提高装置的温度 ③降低装置的压强 ④在装置中装入碱石灰
A.①③ B.②④ C.①④ D.②③
(4)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒气体成分较普通车型下降80%左右,解决了汽车尾气排放给城市环境造成的污染问题。下列物质中不属于上述有害气体的是( )
A.H2O(g) B.NO2和NO
C.CO和SO2 D.碳粒和含铅化合物
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
汽车的发明与使用,是人类智慧的杰出体现,它为人们的生活和生产带来了
极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注,人们开始研
究新的清洁燃料.
(1)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒气体成分较普
通车型下降80%左右,缓解了汽车尾气排放给城市环境造成的污染问题.下列物质
中不属于上述有害气体的是________.
A.CO2和H2 B.NO2和NO
C.CO和SO2 D.C粒和含铅化合物
(2)为了减少大气污染,许多城市推广使用汽车清洁燃料.目前使用的清洁燃料主要
有两类:一类是压缩天然气,另一类是液化石油气.这两类燃料的主要成分都是
________.
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
(3)我国推广使用乙醇汽油,它是在汽油中加入适量乙醇形成的混合燃料.下列叙述
中正确的是________.
A.使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源
B.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型化合物
D.燃烧乙醇汽油可以减少对大气的污染是因为它不含硫元素和氮元素
(4)氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车
备受青睐.我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世
界先进水平,并加快向产业化的目标迈进.氢能具有的优点包括________.
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 5.4 化学农药的发展练习卷(解析版) 题型:选择题
在许多化合物中S可以取代O,取代后的物质仍跟原化合物具有相似的性质,下面是两种有机磷农药的结构简式:
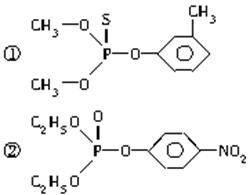
这两种农药在使用过程中不能与下列物质中的哪一种混合使用( )
A.KCl B.Ca(OH)2
C.CO(NH2)2 D.Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
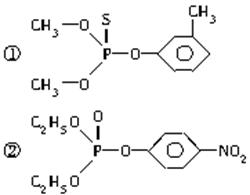
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物。
(1)上述3种气体直接排入空气后会引起酸雨的气体有 (填化学式)。
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:
SO2(g)+NO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g)![]() 2SO3(g) ΔH=a kJ·mol-1
2SO3(g) ΔH=a kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=b kJ·mol-1
2NO2(g) ΔH=b kJ·mol-1
则SO2(g)+NO2(g)![]() SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。
②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:
SO2(g)+NO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
下列事实中不能说明该反应达到平衡状态的是 (选填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
③测得②中反应5 min末到达平衡,此时容器中NO与NO2的体积比为3︰1,则这段时间内SO2的反应速率υ(SO2)= ,此反应在该温度下的平衡常数K= 。
(3)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)![]() CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
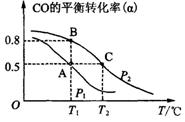
①上述合成甲醇的反应为 反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 。
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 ,理论上通过外电路的电子最多为 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com