
| A. | 联合制碱法中循环使用CO2和NH3,以提高原料利用率 | |
| B. | 硫酸工业中,SO2氧化为SO3时采用常压,因为高压会降低SO2转化率 | |
| C. | 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |
| D. | 炼钢是在高温下利用氧化剂把生铁中过多的碳和其他杂质氧化成气体或炉渣除去 |
分析 A.联合制碱法中氨气没有循环利用;
B.增大压强可以提高SO2的转化率,但是会增大成本;
C.反应物浓度减小,则反应速率会减小;
D.生铁中含有较多的碳,可用氧化而除去,达到炼钢的目的.
解答 解:A.联合制碱法中二氧化碳被循环利用,而氨气没有被循环利用,故A错误;
B.增大压强对SO2的转化率影响不大,同时增大成本,故通常采取采用常压而不是高压,故B错误;
C.合成氨生产过程中将NH3液化分离,导致反应物浓度减小,逆反应速率减小,则平衡向着正向移动,从而提高了N2、H2的转化率,故C错误;
D.降低生铁中含有含碳量,需要加入氧化剂将生铁中过多的碳和其他杂质氧化成气体或炉渣除去,故D正确;
故选D.
点评 本题考查较为综合,涉及工业制硝酸、合成氨、化学平衡的影响等知识,题目难度中等,明确化学平衡的影响因素为解答关键,注意掌握合成氨、工作制硝酸的反应原理,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
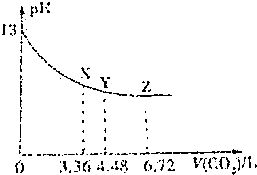
| A. | 该NaOH溶液的浓度为0.1mol/L,体积为6L | |
| B. | X、Y、Z三点对应的溶液中离子的种类不同 | |
| C. | Y点对应的融资中离子浓度关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| D. | Y点对应的溶液中存在着:c(Na+)=2c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中含有少量Na2CO3,可以用澄清石灰水除去 | |
| B. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 | |
| C. | 加水稀释CH3COONa溶液,溶液中的所有离子浓度都减小 | |
| D. | 金属铝的生产是以Al2O3为原料,在熔融状态下进行电解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
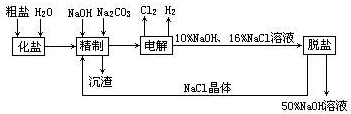
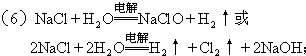 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Mg2+)>c(Mn2+) | |
| B. | c(Mg2+)=c(Mn2+) | |
| C. | c(Mg2+)<c(Mn2+) | |
| D. | 沉淀类型不同,无法用Ksp比较二种离子的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ③④⑤ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在丙烯醛分子中,仅含有一种官能团 | |
| B. | 丙烯醛能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 | |
| C. | 丙烯醛能发生加聚反应,生成高聚物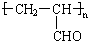 | |
| D. | 等物质的量的丙烯醛和丙醛完全燃烧,消耗等物质的量的O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
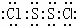 ,二氯化二硫(S2Cl2)所属的晶体类型分子晶体.
,二氯化二硫(S2Cl2)所属的晶体类型分子晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com