
| A. | pH=1的溶液中:Na+、Fe3+、NO3-、I- | |
| B. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Al3+、Cl-、SO42- | |
| C. | c( Al 3+)=0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- |
分析 A.pH=1的溶液,显酸性;
B.水电离出的c(H+)=1×10-12mol•L-1的溶液,为酸或碱溶液;
C.离子之间相互促进水解;
D.加入KSCN溶液显红色的溶液,含铁离子,该组离子之间不反应.
解答 解:A.pH=1的溶液,显酸性,NO3-、I-发生氧化还原反应,不能共存,故A不选;
B.水电离出的c(H+)=1×10-12mol•L-1的溶液,为酸或碱溶液,碱溶液中不能大量存在Al3+,故B不选;
C.Al3+、HCO3-相互促进水解,不能共存,故C不选;
D.加入KSCN溶液显红色的溶液,含铁离子,该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意水解反应、氧化还原反应的判断,题目难度不大.


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:实验题
| 名称 | 相对分子质量 | 沸点/(℃) | 密度/(g/mL) |
| 苯 | 78 | 78 | 0.88 |
| 氯苯 | 112.5 | 132.2 | 1.1 |
| 邻二氯苯 | 147 | 180.4 | 1.3 |

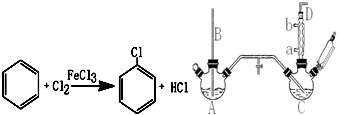
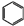 +2HCl+O2$→_{210℃}^{催化剂}$2
+2HCl+O2$→_{210℃}^{催化剂}$2 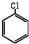 +2 H2O.
+2 H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
| A. | 蒸馏 | B. | 分液 | C. | 过滤 | D. | 蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向容量瓶中加水未到刻度线 | |
| B. | 所用NaOH已经潮解 | |
| C. | 有少量NaOH溶液残留在烧杯里 | |
| D. | 用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
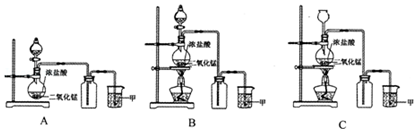
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是用来描述微观粒子的物理量 | |
| B. | 1 mol任何物质都含有Na个原子 | |
| C. | 0.5 mol H2O中含有的原子数目为1.5Na | |
| D. | 64g氧相当于2mol氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
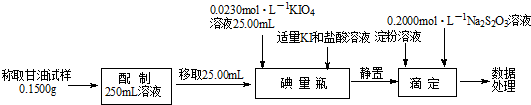
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com