
【题目】下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是

选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
C | N2 | NO2 | HNO3 | ③加热 |
D | C | CO | CO2 | ④灼热炭粉 |
A. A B. B C. C D. D
【答案】C
【解析】A、SiO2和Na2CO3熔融生成Na2SiO3,Na2SiO3和稀盐酸反应生成H2SiO3,H2SiO3分解生成SiO2,涉及的反应为 SiO2+Na2CO3 ![]() Na2SiO3+CO2↑、Na2SiO3+2HCl=2NaCl+H2SiO3↓、H2SiO3
Na2SiO3+CO2↑、Na2SiO3+2HCl=2NaCl+H2SiO3↓、H2SiO3![]() H2O+SiO2,故A正确;B.氯化钠和氨气、二氧化碳反应生成NaHCO3,NaHCO3加热分解生成Na2CO3,Na2CO3和二氧化碳、水反应生成碳酸氢钠,Na2CO3和氯化钙反应生成氯化钠,发生的反应为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl、2NaHCO3
H2O+SiO2,故A正确;B.氯化钠和氨气、二氧化碳反应生成NaHCO3,NaHCO3加热分解生成Na2CO3,Na2CO3和二氧化碳、水反应生成碳酸氢钠,Na2CO3和氯化钙反应生成氯化钠,发生的反应为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl、2NaHCO3![]() Na2CO3+H2O+CO2↑、Na2CO3+H2O+CO2=2NaHCO3、Na2CO3+CaCl2=CaCO3↓+2NaCl,故B正确;C.N2和O2反应生成NO而不能生成NO2;HNO3分解生成NO2、氧气和水,发生的反应为N2+O2
Na2CO3+H2O+CO2↑、Na2CO3+H2O+CO2=2NaHCO3、Na2CO3+CaCl2=CaCO3↓+2NaCl,故B正确;C.N2和O2反应生成NO而不能生成NO2;HNO3分解生成NO2、氧气和水,发生的反应为N2+O2![]() 2NO、3NO2+H2O=2HNO3+NO、4HNO3
2NO、3NO2+H2O=2HNO3+NO、4HNO3![]() 4NO2↑+O2↑+2H2O,故C错误;C.碳不完全燃烧生成CO,CO燃烧生成CO2,CO2和C反应生成CO,CO2和Mg反应生成C,发生的反应为2C+O2
4NO2↑+O2↑+2H2O,故C错误;C.碳不完全燃烧生成CO,CO燃烧生成CO2,CO2和C反应生成CO,CO2和Mg反应生成C,发生的反应为2C+O2![]() 2CO、2CO+O2
2CO、2CO+O2![]() 2CO2、C+CO2
2CO2、C+CO2![]() 2CO、CO2+2Mg
2CO、CO2+2Mg![]() 2MgO+C,故D正确;故选C。
2MgO+C,故D正确;故选C。


科目:高中化学 来源: 题型:
【题目】甲醇、乙二醇、丙三醇中分别加入足量的金属钠产生等体积的氢气(相同条件),则上述三种醇的物质的量之比是( )
A.2:3:6
B.6:3:2
C.4:3:1
D.3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
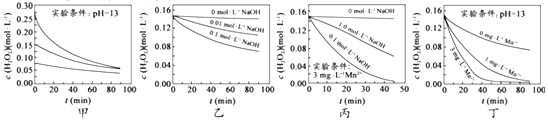
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液PH 越小,H2O2分解速率越快
C. 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项有机化合物的命名或分类正确的是( )
A.2,3﹣二甲基﹣2﹣乙基己烷
B.CH3CH2CH2Cl氯丙烷
C.![]() 属于芳香醇
属于芳香醇
D.![]() 属于芳香化合物
属于芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 微量元素就是可有可无的元素
B. 微量元素主要是指Cu、Fe、B、Mn等
C. 缺少微量元素生命活动要受到影响
D. 微量元素也是生命和非生物界共有的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式为 ,下列关于该化合物的说法不正确的是
,下列关于该化合物的说法不正确的是
A. 该有机物的分子式为C23H24O6
B. 1mol该化合物最多可以与9molH2发生加成反应
C. 既可以使溴的四氯化碳溶液褪色,又可以使酸性KMnO4溶液褪色
D. 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链.其主要工艺如下:
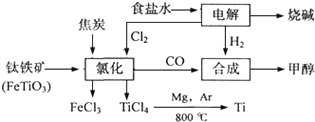
(1)写出钛铁矿经氯化法得到四氯化钛的化学方程式:_____________________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=﹣641kJmol﹣1
②Ti(s)+2Cl2(g)=TiCl4(s);△H=﹣770kJmol﹣1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);△H=___________________________。反应2Mg+TiCl4![]() 2MgCl4+Ti在Ar气氛中进行的理由是_______________________。
2MgCl4+Ti在Ar气氛中进行的理由是_______________________。
(3)在上述产业链中,合成192t甲醇理论上需额外补充H2___________t(不考虑生产过程中物质的任何损失).
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中负极上的电极反应式是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
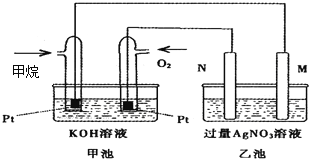
(1)M电极的材料是__________,其电极名称是_____________。
(2)N的电极反应式为____________________________,通入甲烷的电极反应式为______________________________________________,
(3)乙池总反应的化学方程式是_______________________________________________,
(4)在此过程中,乙池中某一电极析出金属银4.32g,甲池中理论上消耗氧气为_____mL(标准状况下),若此时乙池溶液的体积为400mL,则乙池中溶液的H+的浓度为__________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com