
| 温度 | 250 | 300 | 350 |
| K | 2.041 | 0.250 | 0.012 |
分析 (1)利用盖斯定律可以根据已知的反应的热化学方程式求反应2CO+SO2=S+2CO2的焓变,进而写热化学方程式;
(2)①利用三段式法计算出平衡浓度,转化率=$\frac{消耗量}{起始量}$×100%,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,结合平衡常数大小判断反应的温度;
②CO(g)+2H2(g)?CH3OH(g),依据平衡常数随温度变化可知,温度升高,平衡常数减小说明反应是放热反应,在恒容条件下,要提高CO(g)的转化率,可以改变条件使平衡正向进行,注意若只增大CO浓度,平衡向正反应移动,CO的转化率降低;
③合成气进行循环,可以提高原料利用率;
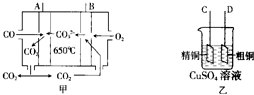
(3)根据CO具有还原性,在负极上发生氧化反应生成CO2,结合电解质书写电极反应式;根据A为负极,B为正极,粗铜精炼时,粗铜作阳极,与电源的正极相连;根据电子得失守恒以及粗铜中除了铜失去电子还有其他金属失去电子;
①根据CO具有还原性,在负极上发生氧化反应生成CO2,结合电解质书写电极反应式;
②根据A为负极,B为正极,粗铜精炼时,粗铜作阳极,与电源的正极相连;
③根据电子得失守恒以及精铜中铜离子得到电子的电极反应来计算,粗铜做阳极含有锌、铁、镍、金、银等,结合电子守恒分析.
解答 解:(1)①C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
②CO2(g)+C(s)=2CO(g)△H2=172.5kJ/mol
③S(s)+O2(g)=SO2(g)△H3=-296.0kJ/mol
根据盖斯定律,①-②-③得到反应的热化学方程式为::
2CO(g)+SO2(g)=S(s)+2CO2(g)△H=△H1-△H2-△H3=-270 kJ•mol-1,
故答案为:2CO(g)+SO2(g)=S(s)+2CO2(g);△H3=-270 kJ•mol-1;
(2)①某温度下,将2molCO(g)和6molH2(g)充入2L的密闭容器中,充分反应后,达到平衡时c(CO)=0.5mol/L,
CO(g)+H2O(g)?CO2(g)+H2(g)
起始浓度(mol/L) 1 3 0 0
转化浓度(mol/L) 0.5 0.5 0.5 0.5
转化浓度(mol/L) 0.5 2.5 0.5 0.5
所以CO的转化率α(CO)=$\frac{0.5mol/L}{1mol/L}$×100%=50%
K=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$=$\frac{0.5×0.5}{0.5×2.5}$=0.2,
反应的温度接近于300°C;
故答案为:50%;300°C;
②CO(g)+2H2(g)?CH3OH(g),依据平衡常数随温度变化可知,温度升高,平衡常数减小说明反应是放热反应,在恒容条件下,要提高CO(g)的转化率,可以改变条件使平衡正向进行;
A.升高温度,平衡向逆反应移动,平衡时CO的转化率减小,故A错误;
B.加入催化剂,缩短到达平衡时间,平衡不移动,CO转化率不变,故B错误;
C.增加CO的浓度,平衡向正反应移动,平衡时CO的转化率减小,故C错误;
D.加入H2加压,平衡向正反应移动,平衡时CO的转化率增大,故D正确;
E.分离出甲醇,平衡向正反应移动,平衡时CO的转化率增大,故E正确.
F.加入惰性气体加压,反应混合物的浓度不变,变化不移动,故F错误;
故选:DE;
③生产过程中,合成气要进行循环,这样可以提高原料利用率,符合经济效益;
故答案为:提高原料利用率;.
(3)①CO具有还原性,在负极上发生氧化反应生成CO2,电极反应式为:CO-2e-+CO32-═2CO2,
故答案为:CO-2e-+CO32-=2CO2;
②因A为负极,B为正极,粗铜精炼时,粗铜作阳极,与电源的正极相连,故选:D;
故答案为:D.
③当消耗标准状况下2.24L CO时,电极反应式:CO-2e-+CO32-=2CO2,失去电子为$\frac{2.24L}{22.4L/mol}$×2=0.2mol,精铜电极电极反应式:Cu2++2e-=Cu,由电子得失守恒可知Cu2+的物质的量为0.1mol,精铜电极的质量增加的质量为:0.1mol×64g/mol=6.4g,粗铜做阳极,其中的铜、锌、镍等金属失电子,粗铜电极理论上减少铜的质量一定小于6.4g;
故答案:小于6.4g.
点评 本题考查了学生热化学方程式的书写,化学反应速率化学平衡影响因素分析判断,电解原理的分析应用等有关知识,综合性强,注意粗铜精炼的原理分析,难度中等.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:选择题

| A. | 视黄醛的分子式为C24H20O | |
| B. | 维生素A分子结构中含有苯环、碳碳双键和羟基 | |
| C. | 维生素A是视黄醛的氧化产物 | |
| D. | 1mol视黄醛在一定条件下最多能与8molH2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 非金属性:N<Si | B. | 稳定性:HF>H2S | ||
| C. | 碱性:Ca(OH)2<Mg(OH)2 | D. | 酸性强弱:H3PO4<H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
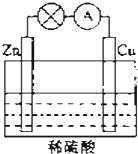 电能是现代社会应用最广泛的能源之一.如图所示的原电池装置中,其负极是Zn,正极上能够观察到的现象是铜片表面产生无色气泡,正极的电极反应式是2H++2e-=H2↑.原电池工作一段时间后,若消耗锌6.5g,则放出气体0.2g.
电能是现代社会应用最广泛的能源之一.如图所示的原电池装置中,其负极是Zn,正极上能够观察到的现象是铜片表面产生无色气泡,正极的电极反应式是2H++2e-=H2↑.原电池工作一段时间后,若消耗锌6.5g,则放出气体0.2g.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,质量为32gO2含有的原子数为2NA | |
| B. | 2L0.1mol/LNaCl溶液中含有NaCl分子数为0.2NA | |
| C. | 78gNa2O2与足量CO2完全反应吗,转移的电子数为2NA | |
| D. | 在25℃,101Pa条件下,11.2L氯气所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1L pH=13的Ba(OH)2溶液中含有OH一的数目为0.2NA | |
| B. | 取50mL 14.0moI.L-l浓硝酸与足量的铜片反应,生成气体分子的数目为0.35NA | |
| C. | 标准状况下,2.24L二氧化硫中含有的电子总数为3.2NA | |
| D. | 28gN2与28g C18O中含有的质子数均为14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| B. | 向硝酸银溶液中加入足量的氨水:Ag++2NH3•H2O═Ag(NH3)2++2H2O | |
| C. | 泡沫灭火器的灭火原理:2Al3++3CO32-+3H20═2Al(OH)3↓+3CO2↑ | |
| D. | 用足量的氨水处理硫酸工业的尾气:SO2+NH3•H2O═NH4++HSO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com