
能正确表示下列反应的离子方程式是( )
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+
C.Ca(HCO3)2溶液与少量NaOH溶液反应:
HCO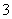 +Ca2++OH-=CaCO3↓+H2O
+Ca2++OH-=CaCO3↓+H2O
D.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
科目:高中化学 来源: 题型:
下列物质的俗称、主要成分的化学式及其用途均正确的是
A.磁铁矿——Fe2O3——炼铁 B.胆矾——CuSO4·5H2O——波尔多液
C.蓝宝石——SiO2——饰品 D.纯碱——NaHCO3——焙制糕点
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验:


请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整。
(2)实验中他们取6.4g铜片和12mL18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:_________________________________________;
实验中若有m g铜参加了反应,则有______mol硫酸被还原,电子转移数目为___。
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是__________(填写字母编号)。
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
__________________________________________________________________。
(3)为了测定消耗硫酸的物质的量,该兴趣小组设计了两个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量。
实际上,方案一、二均不可取。
方案一产生的气体中含有 ,使干燥管增重偏大;也可能由于
,使干燥管增重偏小。
方案二:由于 与氯化钡溶液反应,使测定消耗硫酸的物质的量结果偏大。
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿佛加德罗常数,下列说法正确的是 ( )
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C.14 g氮气中含有7 NA个电子
D.NA个一氧化碳分子和0.5 molCH4所含原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
中国于2011年5月1日禁止面粉添加增白剂。已知增白剂中含有CaO2,其性质与Na2O2性质相似。下列说法错误的是( )
A.CaO2可作供氧剂、强氧化剂
B.等质量的Ca与足量O2反应分别生成CaO和CaO2,转移电子数之比为1︰1
C.CaO2与H2O反应生成Ca(OH)2和O2
D.CaO2与H2O反应的溶液中滴加酚酞,溶液只变红
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250 mL 0.1 mol/L HCl溶液时,下列操作会使配得溶液的物质的量浓度偏大的是( )
A.定容后摇匀,发现液面低于刻度线,再加水至刻度线
B.转移液体后未洗涤烧杯
C.在容量瓶中进行定容时,俯视刻度线
D.配制前洗涤好的容量瓶内有少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分解1 mol H2O2放出热量98 kJ。在含少量I-的溶液中,H2O2分解的机理为
H2 O2+I-—→H2O+IO- 慢
O2+I-—→H2O+IO- 慢
H2O2+IO-—→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
A.反应速率与I-浓度有关
B.IO-也是该反应的催化剂
C.反应活化能等于98 kJ·mol-1
D.v(H2O2)=v(H2O)=v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 18g D2O含有的电子数为10NA
B. 标准状况下,11.2 L SO3中含有的分子数为0.5 NA
C. 7.8 g Na2O2晶体中含有的阴离子数为0.1 NA
D. 常温常压下,44 g CO2气体含有氧原子的个数为2 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com