
【题目】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:


图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为__________________________________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中B原子个数与极性键个数比为____________。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________理论。
(4)三种晶体中熔点最低的是________(填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为____________________________________________________________。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为_______________________________________。
【答案】812O1∶6金属键H3BO3分子间作用力![]() g·cm-3
g·cm-3
【解析】
(1)根据CaF2晶胞结构可知,CaF2晶体中Ca2+的配位数为8,F-的配位数为4,Ca2+和F-个数比为1:2,铜晶体中未标号的铜原子周围最紧邻的铜原子为上层1、2、3,同层的4、5、6、7、8、9,下层的10、11、12;(2) H3BO3晶体中B原子最外层三个电子形成三条共价键,最外层共6个电子,H原子达到2电子稳定结构,只有氧原子形成两条键达到8电子稳定结构。H3BO3晶体是分子晶体,相互之间通过氢键相连,每个B原子形成三条B—O极性键,每个O原子形成一条O—H极性价键;(3)金属键理论把金属键描述为金属原子脱落下来的价电子形成整块晶体的电子气,被所有原子所共用,从而把所有的原子联系在一起;(4)H3BO3晶体是分子晶体,熔点最低,熔化时克服了分子间作用力;(5)一个晶胞中实际拥有的离子数:阳离子数为8×1/8+6×1/2=4,而阴离子为8个,1个晶胞实际拥有4个“CaF2”。
(1)CaF2晶体中Ca2+的配位数为8,F-的配位数为4,Ca2+和F-个数比为1∶2,铜晶体中未标号的铜原子周围最紧邻的铜原子为上层1、2、3,同层的4、5、6、7、8、9,下层的10、11、12,共12个。 (2)图Ⅱ中B原子最外层三个电子形成三条共价键,所以最外层共6个电子,H原子达到2电子稳定结构,只有氧原子形成两条键达到8电子稳定。H3BO3晶体是分子晶体,相互之间通过氢键相连,每个B原子形成三条B—O极性键,每个O原子形成一条O—H极性价键,共6条极性键,B原子个数与极性键个数比为1∶6。 (3)金属键理论把金属键描述为金属原子脱落下来的价电子形成整块晶体的电子气,被所有原子所共用,从而把所有的原子联系在一起,可以用来解释金属键的本质,金属的延展性、导电性、传热性。(4)H3BO3晶体是分子晶体,熔点最低,熔化时克服了分子间作用力。(5)一个晶胞中实际拥有的离子数:阳离子数为8×1/8+6×1/2=4,而阴离子为8个,1个晶胞实际拥有4个“CaF2”,则CaF2晶体的密度为4×78 g·mol-1÷[(![]() a×10-8cm)3×6.02×1023mol-1]≈
a×10-8cm)3×6.02×1023mol-1]≈![]() g·cm-3。
g·cm-3。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO3-被还原为NO),最终溶液体积为1L。下列说法正确的是
A. 所得溶液中c(NO3-)=2.75 mol·L-1
B. 所得溶液中c(Fe2+):c(Fe3+)=1:2
C. 反应后生成NO的体积为33.6 L(标准状况下)
D. 所得溶液中的溶质只有FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
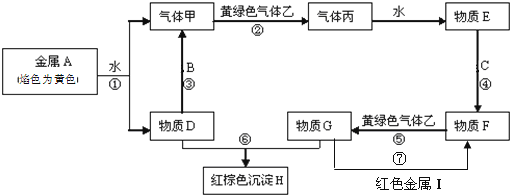
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C__________、H_________。
(2)写出反应③的化学方程式:___________________。
写出反应⑦的化学方程式:___________________。
写出反应⑥的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)实验测得 8 g 液态甲醇(化学式为 CH4O)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出 181.6 kJ 的热量。请写出表示液态甲醇燃烧热的热化学方程式:_______。
(2)发射卫星时常用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,这两种物质反应生成氮气和水蒸气。 已知:①N2(g)+2O2(g)=2NO2(g) ΔH= a kJ/mol;②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH= b kJ/mol。写出肼气体与二氧化氮气体反应的热化学方程式:_______。
II.某学习小组的同学在实验室利用下图装置进行中和热的测定,请回答下列问题:

(1)在其它操作正确的前提下,如果大烧杯不盖硬纸板,求得的中和热 ΔH 将_______(填“偏大”、“偏小” 或“无影响”)。
(2)取 50 mL 0.50 mol/L NaOH 溶液和 30 mL 0.50 mol/L 硫酸溶液进行实验,实验数据如下表。
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.5 | 26.7 | 26.6 | 30.1 | |
2 | 26.0 | 26.4 | 26.2 | 30.3 | |
3 | 25.9 | 25.9 | 25.9 | 30.2 | |
4 | 26.4 | 26.2 | 26.3 | 30.5 | |
①表中的温度差的平均值为_____℃。
②近似认为 0.50 mol/L NaOH溶液和 0.50 mol/L硫酸溶液的密度都是 1 g·cm-3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热 ΔH=_____kJ/mol (保留到小数点后一位)。
③实验中改用 60 mL0.50 mol/L 盐酸跟 50 mL 0.55 mol/L 氢氧化钠进行反应,若其它实验操作均正确,则与上述实验相比,所放出的热量_____(填“相等”或“不相等”,下同),所求得的中和热_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是( )

A.2F2+2H2O═4HF+O2
B.AgNO3+NaCl═AgCl↓+NaNO3
C.3CO+Fe2O3 ![]() 2Fe+3CO2
2Fe+3CO2
D.MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的应用广泛,回答下列问题:
(1)碘盐中含有KIO3,KIO3中碘元素的化合价是____________。
(2)84消毒液的有效成分是____________(填“NaCl”或“NaClO”)。
(3)高温下Fe2O3与CO反应是工业上炼铁的原理,该原理的化学反应方程式为____________,反应中Fe2O3做________(填“氧化剂”或“还原剂”)。
(4)实验室用NaOH溶液吸收含SO2的尾气,该反应的离子方程式为____________,SO2属于____________(填“酸性氧化物”或“碱性氧化物”),SO2能使品红溶液褪色,说明SO2具有的性质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. 向![]() 溶液中滴加氨水至过量:
溶液中滴加氨水至过量:![]()
B. 向![]() 悬浊液中滴加
悬浊液中滴加![]() 溶液:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
溶液:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
C. 向![]() 溶液中加入足量稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
溶液中加入足量稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
D. 向苯酚钠溶液中通入少量![]() 气体:2C6H5O-+CO2+H2O=2C6H5OH+CO32-
气体:2C6H5O-+CO2+H2O=2C6H5OH+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。

请回答下列问题:
(1)F的化学名称是________,⑤的反应类型是________。
(2)E中含有的官能团是________(写名称),D聚合生成高分子化合物的结构简式为________。
(3)将反应③得到的产物与O2在催化剂、加热的条件下反应可得D,写出反应④的化学方程式________。
(4)④、⑤两步能否颠倒?________(填“能”或“否”)理由是________。
(5)与A具有含有相同官能团的芳香化合物的同分异构体还有________种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为________。
(6)参照有机物W的上述合成路线,以M和CH3Cl为原料制备F的合成路线(无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+C(g)===D(g);ΔH=-Q1kJ/mol,B(g)+C(g)===E(g);ΔH=-Q2kJ/mol,Q1、Q2均大于0,且Q1>Q2,若A与B组成的混合气体 1mol与足量的C反应,放热为Q3kJ,则原混合气体中A与B物质的量之比为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com