
【题目】叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,其中氢叠氮酸(HN3)是一种弱酸,分子结构示意图可表示为:
联氨被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2=2H2O+HN3
它的酸性类似于醋酸,微弱电离出H+和N。试回答下列问题:
(1)下列有关说法正确的是_____________(选填序号)。
A.HN3中含有5个σ键
B.HN3中三个氮原子采用的都是sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)沸点高达113.5℃,说明肼分子间可形成氢键
(2)叠氮化物能与Fe3+及Cu2+及Co3+等形成配合物,如:Co[(N3)(NH3)5]SO4 , 在该配合物中钴显价,根据价层互斥理论可知SO空间形状为 , 写出钴原子在基态时的核外电子排布式。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是_____(选填序号)
A.NaN3与KN3结构类似,前者晶格能较小
B.钠晶胞结构如上图,晶胞中分摊2个钠原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(4)与N互为等电子体的分子有(举2例)
(5)人造立方氮化硼的硬度仅次于金刚石而远远高于其它材料,因此它与金刚石统称为超硬材料。立方氮化硼晶胞如下图所示,试分析: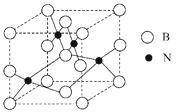
①该晶体的类别为晶体。
②晶体中每个N同时吸引个B。
③设该晶体的摩尔质量为M g·mol-1 , 晶体的密度
为ρg·cm-3 , 阿伏加德罗常数的值为NA , 则晶体
中两个距离最近的B之间的距离为cm。
【答案】
(1)C,D
(2)+3;正四面体;1s22s22p63s23p63d74S2或[Ar] 3d74S2
(3)B,C
(4)N2O、CO2、CS2、BeF2等
(5)原子;4;![]()
【解析】解:(1)A.共价单键为σ键,共价双键中1个是σ键、1个是π键,所以该分子中含有3个σ键,故错误;
B.HN3中三个N原子价层电子对个数不相同,所以其杂化方式不同,故错误;
C.分子正负电荷重心不重合的为极性分子,这几种分子正负电荷重心都不重合,为极性分子,故正确;
D.形成氢键的氢化物熔沸点较高,该氢化物熔沸点大于水,含有氢键,故正确;
故选CD;
(2) 该配合物中叠氮酸根离子为-1价、硫酸根离子为-2价,根据化合物中各元素化合价的代数和为0知,Co元素化合价为+3价;硫酸根离子价层电子对个数是4 且不含孤电子对,根据价层电子对互斥理论判断硫酸根离子空间构型为正四面体形;Co是27号元素,其原子核外有27个电子,根据构造原理书写其基态原子核 外电子排布式为1s22s22p63s23p63d74s2或[Ar]3d74s2 ,
所以答案是:+3;正四面体;1s22s22p63s23p63d74s2或[Ar]3d74s2;
(3)A.NaN3与KN3结构类似,且二者都是离子晶体,晶格能与离子半径成反比,钾离子半径大于钠离子,所以前者晶格能大于后者,故错误;
B.晶胞中Na原子个数=8×![]() +1=2,故正确;
+1=2,故正确;
C.同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族第一电离能大于其相邻元素,所以第一电离能N>O,故正确;
D.氮气分子中含有氮氮三键,键能较大,性质较稳定,故错误;
故选BC;
(4)原子个数相等价电子数相等的微粒互为等电子体,与N3-互为等电子体的分子有N2O、CO2、CS2、BeF2等,所以答案是:N2O、CO2、CS2、BeF2等;
(5)①原子晶体硬度大,该晶体硬度大,所以为原子晶体,所以答案是:原子;
②每个N原子同时吸引4个B原子,所以其配位数是4,所以答案是:4;
③晶体中两个距离最近的B之间的距离为晶胞棱长的![]() 倍,晶胞棱长=
倍,晶胞棱长=![]() ,
,
则晶体中两个距离最近的B之间的距离=![]() ×
×![]() cm=
cm=![]() ×
×![]() cm=
cm=![]() cm,
cm,
所以答案是:![]() .
.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)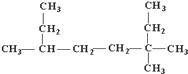 的名称为;
的名称为;
(2)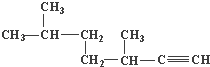 的名称为;
的名称为;
(3)2,4﹣二氯甲苯的结构简式为;
(4)某物质结构如右图 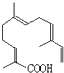 所示,分子式为;该物质可以与下列(填序号)发生反应.
所示,分子式为;该物质可以与下列(填序号)发生反应.
A.KMnO4酸性溶液 B.氢气 C.溴水 D.NaOH溶液
(5)![]() 中含有的官能团的名称为 , .
中含有的官能团的名称为 , .
(6)在戊烷的各种同分异构体中,核磁共振氢谱只有一个吸收峰的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,之后改滴试剂B,所得沉淀y mol与试剂体积V(ml)间的关系.以下结论不正确的是( ) 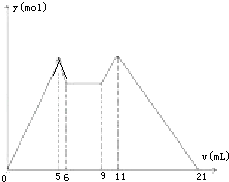
A.A是盐酸,B是NaOH,且C(NaOH)=2C(HCl)
B.原混合液中,C(Al3+):C(Mg2+):C(Cl﹣)=1:1:5
C.A是NaOH,B是盐酸,且C(NaOH):C(HCl)=2:1
D.从6到9,相应离子反应式H++OH﹣═H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取硝酸铵的流程图如下,请回答下列问题: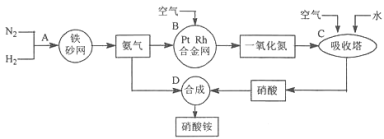
(1)合成氨的工业设备名称是 , 设备中设置热交换器的目的是;此生产过程中,N2与H2合成NH3所用的催化剂是;生产中原料气必须进行脱硫,目的是。
(2)吸收塔中的反应为 , 从生产流程看,吸收塔中需要补充空气,其原因是。
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下三种方法处理:
方法一:碱吸收法:NO+NO2+2NaOH=2NaNO2+H2O,2NO2+Na2CO3=NaNO2+NaNO3+CO2
方法二:氨还原法:8NH3+6NO2=7N2+12H2O(该反应放热,NO也有类似的反应)
方法三:甲烷吸收法:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) △H=+867kJ·mol-1(NO也有类似的反应)上述三种方法中方法一最大的缺点是;方法三和方法二相比,优点是 , 缺点是。
(4)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用的NH3的质量占总耗NH3质量(不考虑其他损耗)的%(保留三位有效数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( )
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 石蕊试液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝 | Cl2具有氧化性 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去). A ![]() B
B ![]() C
C ![]() D
D
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体. ①D的化学式是;
②在工业生产中,B气体的大量排放被雨水吸收后形成了而污染了环境.
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 , 用化学方程式表示该物质与水的反应 . 将C长期露置于空气中,最后将变成物质D,D的化学式为 . 现在有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .
(3)若C是红棕色气体.图是实验室制取A气体的装置: 
①写出实验室制取A的化学方程式 .
②为了检验氨气是否集满,可将 , 则证明已收集满.D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~M有如图转化关系,A与F分子中含碳原子数相同,均能与NaHCO3溶液反应,且A中含一个卤素原子,F的分子式为C9H10O2;D能发生银镜反应;M与NaOH溶液反应后的产物,其苯环上一氯代物只有一种.
已知: 
请回答:
(1)B、F的结构简式分别为、;
(2)反应①⑦中,属于消去反应的是(填反应序号);
(3)D发生银镜反应的化学方程式为;反应⑦的化学方程式为。
(4)A的相对分子质量在180260之间,从以上转化中不能确认A中含有哪种卤素原子,确定该官能团的实验步骤和现象为;
(5)符合下列条件F的同分异构体共有种.a.能发生银镜反应b.能与FeCl3溶液发生显色反应c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.活化分子间的碰撞一定能发生化学反应
B.升高温度时,化学反应速率加快,主要原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.自发进行的反应一定迅速
D.凡是熵增加的过程都是自发过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的下列叙述中,正确的是 ( )
A. 离子化合物不能含共价键 B. 共价化合物可能含离子键
C. 离子化合物中只含离子键 D. 共价化合物中不含离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com