
 A”¢B”¢C”¢D”¢EĪåÖÖ»ÆŗĻĪļ£¬¾łŗ¬ÓŠÄ³ÖÖ³£¼ūŌŖĖŲ£¬ĖüĆĒµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĘäÖŠAĪŖ³ĪĒåČÜŅŗ£¬CĪŖÄŃČܵİ×É«¹ĢĢ壬EŌņŅ×ČÜÓŚĖ®£¬ČōČ”AČÜŅŗ×ĘÉÕ£¬ŃęÉ«·“Ó¦ĪŖĒ³×ĻÉ«£ØĶø¹żĄ¶É«īܲ£Į§£©£®
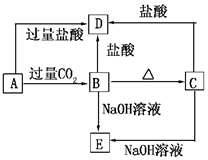
A”¢B”¢C”¢D”¢EĪåÖÖ»ÆŗĻĪļ£¬¾łŗ¬ÓŠÄ³ÖÖ³£¼ūŌŖĖŲ£¬ĖüĆĒµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĘäÖŠAĪŖ³ĪĒåČÜŅŗ£¬CĪŖÄŃČܵİ×É«¹ĢĢ壬EŌņŅ×ČÜÓŚĖ®£¬ČōČ”AČÜŅŗ×ĘÉÕ£¬ŃęÉ«·“Ó¦ĪŖĒ³×ĻÉ«£ØĶø¹żĄ¶É«īܲ£Į§£©£®·ÖĪö B”¢C¶¼¼ČÄÜÓėŃĪĖį·“Ó¦ÓÖÄÜÓėNaOHČÜŅŗ·“Ó¦£¬Ó¦ĪŖĮ½ŠŌ»ÆŗĻĪļ£¬ŅņB¼ÓČČ·Ö½āæÉÉś³ÉC£¬ŌņæÉÖŖBĪŖAl£ØOH£©3£¬CĪŖA12O3£¬ŌņDĪŖAlCl3£¬EĪŖNaAlO2£¬ČōČ”AČÜŅŗ×ĘÉÕ£¬ŃęÉ«·“Ó¦ĪŖ×ĻÉ«£ØĶø¹żĄ¶É«īܲ£Į§Ę¬£©£¬ĖµĆ÷AÖŠŗ¬ÓŠKŌŖĖŲ£¬AÄÜÓė¶žŃõ»ÆĢ¼·“Ӧɜ³ÉAl£ØOH£©3£¬ŌņAÓ¦ĪŖKAlO2£¬½įŗĻ¶ŌÓ¦ĪļÖŹµÄŠŌÖŹ½ā“šøĆĢā£®
½ā“š ½ā£ŗ£Ø1£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬A”¢B”¢C”¢D”¢E·Ö±šŹĒKAlO2”¢Al£ØOH£©3”¢A12O3”¢AlCl3”¢NaAlO2£¬
¹Ź“š°øĪŖ£ŗKAlO2£»Al£ØOH£©3£»A12O3£»AlCl3£»NaAlO2£»
£Ø2£©A”śBµÄ·“Ó¦ĪŖAlO2-ŗĶAl£ØOH£©3µÄ×Ŗ»Æ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£¬
A”śDµÄ·“Ó¦ĪŖAlO2-ŗĶAl3+µÄ×Ŗ»Æ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAlO2-+4H+=Al3++2H2O£¬
¹Ź“š°øĪŖ£ŗAlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£»AlO2-+4H+=Al3++2H2O£®
£Ø3£©C”śEµÄ·“Ó¦ĪŖŃõ»ÆĀĮČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗAl2O3+2NaOH=2NaAlO2+H2O£¬
¹Ź“š°øĪŖ£ŗAl2O3+2NaOH=2NaAlO2+H2O£»
µćĘĄ ±¾Ģāæ¼²éĮĖĀĮ¼°Ęä»ÆŗĻĪļÖ®¼äµÄ×Ŗ»Æ£¬øł¾ŻBÄÜŗĶĒæĖį”¢Ēæ¼ī·“Ó¦ĒŅ¼ÓČČŅ×·Ö½āĶʶĻÖŖ£¬BŹĒĒāŃõ»ÆĀĮ£¬ŌŁ½įŗĻĪļÖŹµÄ·“Ó¦Ģõ¼ž”¢·“Ó¦ĪļĄ“·ÖĪö½ā“š£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāĘ«ĀĮĖįøłĄė×ÓŗĶĢ¼ĖįøłĄė×Ó²»Äܹ²“ę£¬ĪŖŅדķµć£®


 ½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø
æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®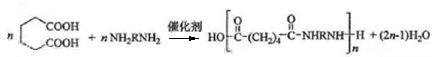 £®
£®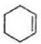 $\stackrel{Br_{2}}{”ś}$
$\stackrel{Br_{2}}{”ś}$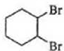 $”ś_{”÷}^{NaOH”¢“¼}$
$”ś_{”÷}^{NaOH”¢“¼}$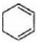 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
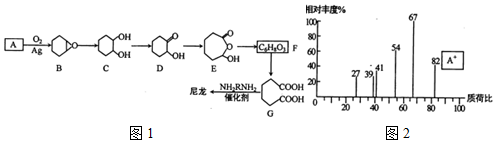
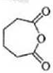
| A£® | C7H16Ö÷Į“ÉĻÓŠ5øöĢ¼Ō×ÓµÄĶ¬·ÖŅģ¹¹ĢåÓŠ5ÖÖ | |
| B£® | °“ĻµĶ³ĆüĆū·Ø£¬»ÆŗĻĪļµÄĆū³ĘŹĒ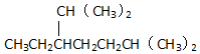 2£¬6-¶ž¼×»ł-3-ŅŅ»łøżĶé 2£¬6-¶ž¼×»ł-3-ŅŅ»łøżĶé | |
| C£® | ŅŅČ²·Ö×ÓµÄĒņ¹÷Ä£ŠĶ£ŗ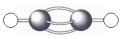 | |
| D£® | Ā±“śĢž¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗøł¾ŻÉś³ÉµÄĀ±»ÆŅų³ĮµķŃÕÉ«¼ģŃéĀ±Ō×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
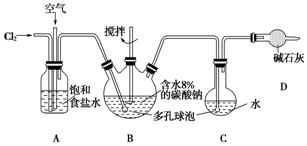
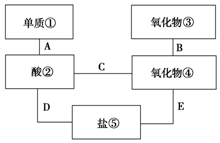 ĻÖÓŠĻ”ĮņĖį”¢“æ¼ī”¢¶žŃõ»ÆĢ¼”¢Ķʬ”¢Ź³ŃĪ”¢ÉśŹÆ»Ņ”¢ĢśĘ¬ŗĶľĢæ·Ū8ÖÖĪļÖŹ£®
ĻÖÓŠĻ”ĮņĖį”¢“æ¼ī”¢¶žŃõ»ÆĢ¼”¢Ķʬ”¢Ź³ŃĪ”¢ÉśŹÆ»Ņ”¢ĢśĘ¬ŗĶľĢæ·Ū8ÖÖĪļÖŹ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
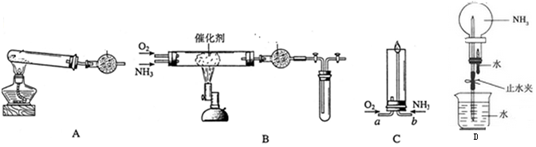
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com