
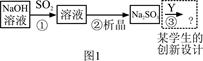
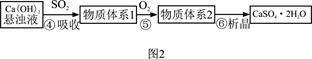
| ŹŌ ¼Į | Ca(OH)2 | NaOH |
| ¼Ūøń£ØŌŖ/kg£© | 0.36 | 2.9 |
| ĪüŹÕSO2µÄ³É±¾£ØŌŖ/mol£© | 0.027 | 0.232 |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
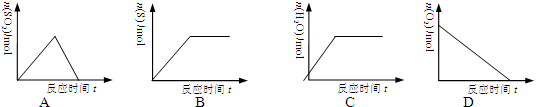
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ś¢Ü | B£®¢Ś¢Ū¢Ż | C£®¢Ś¢Ü¢Ż¢Ž | D£®¢Ł¢Ś¢Ū¢Ü¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŗĶĶ·“Ó¦ÖŠ¶¼±ķĻÖ³öĒæŃõ»ÆŠŌŗĶĖįŠŌ |
| B£®·Ö±šĀ¶ÖĆŌŚæÕĘųÖŠ£¬ČŻĘ÷ÄŚČÜÖŹµÄĪļÖŹµÄĮæÅØ¶Č¶¼½µµĶ |
| C£®¶¼æÉŅŌ“¢“ęÓŚĀĮÖĘ²Ū¹ŽÖŠ |
| D£®¶¼ŹĒ³£ÓƵÄøÉŌļ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®SO2Ź¹äåĖ®ĶŹÉ«£¬ĻŌŹ¾ĮĖSO2µÄĘư׊Ō |
| B£®SO2Ź¹äåĖ®ĶŹÉ«£¬ĻŌŹ¾ĮĖSO2µÄ»¹ŌŠŌ |
| C£®“ÓäåĖ®ÖŠĢįČ”µ„ÖŹä壬æÉŅŌÓĆŅŅ“¼½ųŠŠŻĶČ” |
| D£®SO2ŹĒŠĪ³ÉĖįÓźµÄĪØŅ»ĪŪČ¾Īļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
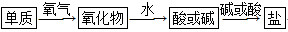
| A£®ĀČ | B£®Įņ | C£®ĀĮ | D£®Ģś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĶÓėĻ”ĮņĖį,ĶÓėÅØĮņĖį |
| B£®ĢśÓėĻ”ĮņĖį,ĢśÓėÅØĮņĖį |
| C£®Įņ»ÆÄĘÓėĻ”ĮņĖį,ŃĒĮņĖįÄĘÓėĻ”ĮņĖį |
| D£®Įņ»ÆÄĘÓėĻ”ĮņĖį,Įņ»ÆÄĘÓėĻ”ŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| A£®Ba(NO3)2 | B£®BaCl2 | C£®Ba(OH)2 | D£®ČÜÓŠNH3µÄBaCl2ČÜŅŗ |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®1”Ć1 | B£®1”Ć2 | C£®2”Ć3 | D£®4”Ć3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com