
 =
=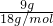 =0.5mol;
=0.5mol; NA=
NA=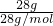 NA=NA;
NA=NA; Vm,同温同压下,Vm相同,NA是常数,所以体积之比等于分子数之比,故为1:1;
Vm,同温同压下,Vm相同,NA是常数,所以体积之比等于分子数之比,故为1:1; Vm得,其体积比为3:2.
Vm得,其体积比为3:2. 、N=nNA=
、N=nNA= NA计算;
NA计算; Vm判断,先根据原子数计算分子数,再根据V=n Vm=
Vm判断,先根据原子数计算分子数,再根据V=n Vm= Vm判断体积比;
Vm判断体积比;

科目:高中化学 来源: 题型:
(15分)
(1)电解精炼铜阳极的主要反应是 ,还会发生的反应有 (任写一个)。
(2)电解精炼铜的阳极泥中含有铜和金、银等贵重金属及稀有金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:
请回答下列问题:
①各步生产流程中都涉及了同一种分离方法,实验室中不能用这种方法来分离液态胶体中分散质与分散剂的原因是 。
②用硝酸处理固体B中碳酸铅的离子方程式是 。
③反应I中肼(N2H4)的作用是 。
④固体C用盐酸、食盐和氯酸钠混合溶液处理后得到H2PtCl6、AuCl3、PdCl2。反应中每消耗lmol氧化剂要转移 mol e-;在AuCl3溶液中通入SO2生成单质金,当生成19.7gAu时,25℃和101kPa下反应消耗 L SO2(此条件下的气体摩尔体积为24.5L/mol)。
查看答案和解析>>
科目:高中化学 来源:2012届安徽省知名省级示范高中高三第一次统考理科综合试卷化学部分(解析版) 题型:填空题
(15分)
(1)电解精炼铜阳极的主要反应是 ,还会发生的反应有 (任写一个)。
(2)电解精炼铜的阳极泥中含有铜和金、银等贵重金属及稀有金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下: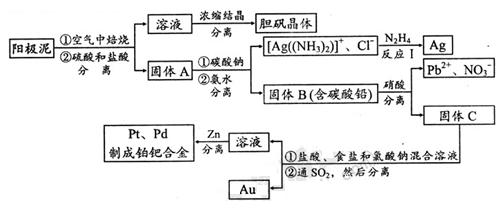
请回答下列问题:
①各步生产流程中都涉及了同一种分离方法,实验室中不能用这种方法来分离液态胶体中分散质与分散剂的原因是 。
②用硝酸处理固体B中碳酸铅的离子方程式是 。
③反应I中肼(N2H4)的作用是 。
④固体C用盐酸、食盐和氯酸钠混合溶液处理后得到H2PtCl6、AuCl3、PdCl2。反应中每消耗lmol氧化剂要转移 mol e-;在AuCl3溶液中通入SO2生成单质金,当生成19.7gAu时,25℃和101kPa下反应消耗 L SO2(此条件下的气体摩尔体积为24.5L/mol)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省高三第一次统考理科综合试卷化学部分(解析版) 题型:填空题
(15分)
(1)电解精炼铜阳极的主要反应是 ,还会发生的反应有 (任写一个)。
(2)电解精炼铜的阳极泥中含有铜和金、银等贵重金属及稀有金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:

请回答下列问题:
①各步生产流程中都涉及了同一种分离方法,实验室中不能用这种方法来分离液态胶体中分散质与分散剂的原因是 。
②用硝酸处理固体B中碳酸铅的离子方程式是 。
③反应I中肼(N2H4)的作用是 。
④固体C用盐酸、食盐和氯酸钠混合溶液处理后得到H2PtCl6、AuCl3、PdCl2。反应中每消耗lmol氧化剂要转移 mol e-;在AuCl3溶液中通入SO2生成单质金,当生成19.7gAu时,25℃和101kPa下反应消耗 L SO2(此条件下的气体摩尔体积为24.5L/mol)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com