
| ��;��Ӧ | �����������ֵ����� |
| ��1����ϡ�����п�������� | |
| ��2����Ũ�����ʳ�ι������Ȼ��� | |
| ��3����ϡ����ϴ���Թܱ��ϸ��ŵ��� | |
| ��4��Ũ���ᡢŨ������ø�ƿ���� | |
| ��5�����õ�Ũ�����Ի�ɫ | |
| ��6����Ũ����ƿ��ʱ��ƿ���а������� | |
| ��7�����ڵ�Ũ���ᣬ����һ��ʱ���������� | |
| ��8��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬���� | |
| ��9��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬����ɫ | �� |
���� ϡ����������ԣ�Ũ��������ѻӷ��ԣ���ˮ�ԡ���ˮ���Լ�ǿ�����ԣ�Ũ���ᡢϡ���ᶼ���������ԣ�Ũ���������Ա�ϡ����ǿ���Դ˽����⣮
��� �⣺��1����ϡ�����п������������Ӧ��ϡ�������Ϊǿ���ԣ�
��2����Ũ�����ʳ�ι������Ȼ��⣬�����Ȼ����ӷ���Ũ������ָ߷е��ԣ�
��3����ϡ����ϴ���Թܱ��ϸ��ŵ�����������������NO��ϡ����������Ժ������ԣ�
��4��Ũ���ᡢŨ������ø�ƿ���ˣ������ۻ���Ӧ������ǿ�����ԣ�
��5�����õ�Ũ�����Ի�ɫ�������ֽ⣬���ֲ��ȶ��ԣ�
��6����Ũ����ƿ��ʱ��ƿ���а������ɣ�˵�������ӷ���
��7�����ڵ�Ũ���ᣬ����һ��ʱ���������������������ˮ�ԣ�
��8��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬���ڣ�����Ũ��������Ժ���ˮ�ԣ�
��9��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬����ɫ��Ũ����������Ժ�ǿ�����ԣ�
�ʴ�Ϊ��
| ��;��Ӧ | �����������ֵ����� |
| ��1����ϡ�����п�������� | �� |
| ��2����Ũ�����ʳ�ι������Ȼ��� | �� |
| ��3����ϡ����ϴ���Թܱ��ϸ��ŵ��� | �ڢ� |
| ��4��Ũ���ᡢŨ������ø�ƿ���� | �� |
| ��5�����õ�Ũ�����Ի�ɫ | �� |
| ��6����Ũ����ƿ��ʱ��ƿ���а������� | �� |
| ��7�����ڵ�Ũ���ᣬ����һ��ʱ���������� | �� |
| ��8��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬���� | �ڢ� |
| ��9��Ũ�����ʹʪ�����ɫʯ����ֽ�ȱ�죬����ɫ | �ڢ� |
���� ���⿼����Ũ���ᡢ��������ʣ�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������ע��Ũ���������ᣬ�������ԣ�������ˮ�ԡ���ˮ�Ժ�ǿ�����ԣ�ע����ˮ�Ժ���ˮ�Ե�������Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100mL12Lmol•L-1Ũ����������MnO2���ȣ�ת�Ƶĵ�����Ϊ0.6NA | |
| B�� | 1mol•L-1��NaClO��Һ�к���ClO-����ĿΪС��NA | |
| C�� | ��״���£�22.4LNO��11.2LO2��Ϻ�����ķ�������ΪNA | |
| D�� | O2��O3�Ļ���ﹲ3.2g������������ԭ����һ��Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.8 mol | B�� | 0.6 mol | C�� | 0.4 mol | D�� | 0.2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 11.4g | B�� | 14.8g | C�� | 205g | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3��10���ӷ��ӣ��������� | |
| B�� | NH3��������ˮ��������Ȫʵ�飻������Һ����Һ������������� | |
| C�� | �����Ƿǵ���ʣ���ˮ�ǵ���� | |
| D�� | մ��Ũ����IJ������������ɲ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4CO+Fe3O4$\frac{\underline{\;����\;}}{\;}$Fe+4CO2 | B�� | 2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2�� | ||
| C�� | Zn+H2SO4�TZnSO4+H2�� | D�� | CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
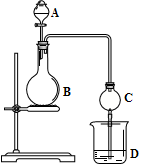 ��ѧʵ���У�ͬһ��װ�ÿ������ڲ�ͬ��ʵ�飬����ͼ��ʵ��װ�ã�B�п�Ϊ�����Һ�壬�ɼ��ȣ���
��ѧʵ���У�ͬһ��װ�ÿ������ڲ�ͬ��ʵ�飬����ͼ��ʵ��װ�ã�B�п�Ϊ�����Һ�壬�ɼ��ȣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L�Ҵ��з�����ΪNA | |
| B�� | ����NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ22.4L | |
| C�� | 1.8g��NH4+�к��еĵ�����Ϊ1.1NA | |
| D�� | ��1 L 2 mol/L�������У�����2NA���Ȼ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com