

| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
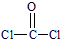
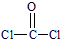
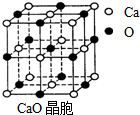 价键是
价键是查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
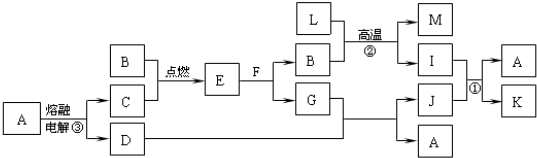
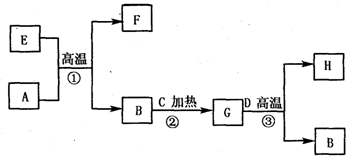 如图所示是电子工业中某原料的生产流程.其中反应②③你可能不熟悉,其目的是为了提纯B;物质A~H均由短周期元素构成;G是五原子分子;A~D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液是一种强酸.
如图所示是电子工业中某原料的生产流程.其中反应②③你可能不熟悉,其目的是为了提纯B;物质A~H均由短周期元素构成;G是五原子分子;A~D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液是一种强酸.查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 4.2 材料组成的优化练习卷(解析版) 题型:推断题
如图所示是电子工业中某原料的生产流程。其中反应②③你可能不熟悉,其目的是为了提纯B;物质A~H均由短周期元素构成;G是五原子分子;A~D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液是一种强酸。
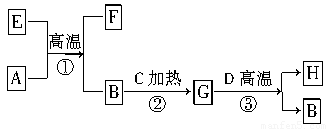
请回答下列问题:
(1)H的电子式________;G的化学式为________。
(2)③所属的反应类型是________。
(3)反应①的化学方程式为_______________________________________。
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com