
下列物质含有离子键的是( )
|
| A. | Cl2 | B. | NaCl | C. | CO2 | D. | H2O |
科目:高中化学 来源: 题型:
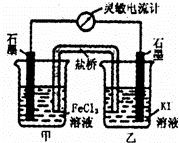
控制适合的条件,将反应2Fe3++2I﹣⇌2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )
|
| A. | 反应开始时,乙中石墨电极上发生氧化反应 |
|
| B. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
|
| C. | 电流计读数为零时,反应达到化学平衡状态 |
|
| D. | 反应开始时,甲中石墨电极上Fe3+被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一特点科学家发明了电动势(E)法测水泥初凝时间,此法的原理如图所示。
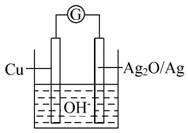
反应的总方程式为2Cu+Ag2O====Cu2O+2Ag。下列有关说法不正确的是 ( )
A.工业上制备普通水泥的主要原料是黏土和石灰石
B.测量原理装置图中,Ag2O/Ag极发生氧化反应
C.负极的电极反应式为2Cu+2OH--2e-====Cu2O+H2O
D.在水泥固化过程中,由于自由水分子的减少,溶液中各离子浓度的变化导致电动势变化
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:
。
 (2)如图为钠高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS====Na2Sx,正极的电极反应式为 。
(2)如图为钠高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS====Na2Sx,正极的电极反应式为 。
M(由Na2O和Al2O3制得)的两个作用是 。
与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
(3)以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为 ,正极的反应式为 。理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为 (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比,甲醇的燃烧热为ΔH=-726.5 kJ·mol-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
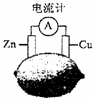
将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转.下列针对该装置的说法正确的是( )
|
| A. | 将电能转换为化学能 | B. | 电子由铜片流出 |
|
| C. | 锌片是负极 | D. | 铜片逐渐被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
今年1月12日,我国3名潜水员圆满完成首次300米饱和潜水作业,实现“下五洋捉鳖”的壮举.
①潜水员乘坐的潜水钟以钢铁为主要制造材料.钢铁容易在潮湿空气中发生电化学腐蚀,其负极的电极反应式是 , .
②潜水员需要均衡的膳食结构.糖类、油脂、蛋白质都能为人体提供能量.某品牌高钙梳打的配料标签如右图所示.在所列配料中,富含糖类的是 ,植物油在体内水解最终产物是高级脂肪酸和 .碳酸氢钠、碳酸钙可调节人体内的过多的胃酸,写出碳酸钙与胃酸反应的离子方程式为 .
③运载潜水钟的母船会产生大量废水和垃圾.科学实验的含汞离子废水 需要处理后再排放,可加入适量的硫化钠溶液,使汞离子变成 (填化学式)沉淀而除去.

查看答案和解析>>
科目:高中化学 来源: 题型:
| Y | Z | R |
| W |
下表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法正确的是( )
A.五种元素的原子最外层电子数一定都大于2
B.X、Z原子序数可能相差18
C.Z可能是氯元素
D.Z的氧化物与X单质不可能发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
以化学反应原理为依据,以实验室研究为基础,可以实现许多化工生产。
I分解水制取氢气的工业制法之一是“硫-碘循环法”,主要涉及下列反应:

分析上述反应,下列判断正确的是____。
循环过程中产生1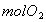 的同时产生
的同时产生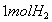
反应①中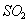 还原性比
还原性比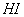 强
强
循环过程中需补充
反应③易在常温下进行
在一定温度下,向2L密闭容器中加入 ,发生反应②.物质的量随时间的变
,发生反应②.物质的量随时间的变 化如图所示。
化如图所示。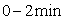 内的平均反应速率
内的平均反应速率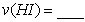
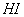 的转化率=_______
的转化率=_______
恒温恒容条件下,硫发生转化的反应过程和能量关系如图所示。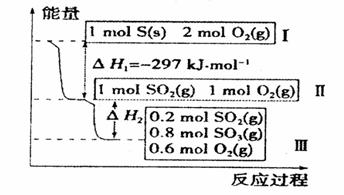 请回答下列问题:
请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式_______;
②恒温恒容时,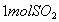 和
和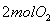 充分反应,放出热量的数值比
充分反应,放出热量的数值比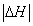 _____(填“大”、“小”或“相等”)
_____(填“大”、“小”或“相等”)
II.氮化硅(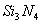 )是一种新型陶瓷材料,工业上有石英与焦炭在高温的氮气流中,通过以下反应制得:
)是一种新型陶瓷材料,工业上有石英与焦炭在高温的氮气流中,通过以下反应制得:

该反应平衡常数的表达式为K=_______.升高温度,其平衡常数
_________(填“增大”、“减少”或“不变”)。
(2)该化学反应速率与反应时间的关系如图所示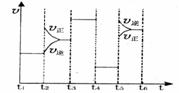
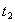 时引
时引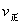 起突变的原因是_____,
起突变的原因是_____,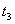 引起变化的因素是_____,
引起变化的因素是_____,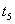 时引
时引 小变化、
小变化、 大变化的原因是_________.
大变化的原因是_________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com