
常温下,下列各组离子在指定溶液中一定能大量共存的是 ( )
A.0.1 mol·L-1 FeCl3溶液:K+、NH4+、I-、SCN-
B.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、NO3-、Cl-
C.0.1 mol·L-1 NaOH溶液:K+、Na+、SO42-、CO32-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
科目:高中化学 来源: 题型:
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在放电过程中的总反应方程式是:NiOOH + MH === Ni(OH)2 + M,下列说法错误的是
A.放电过程中负极的电极反应式:MH + OH--e-=== H2O + M
B.放电过程中OH-从正极向负极迁移
C.放电时若有1 mol M生成,则转移的电子数目为NA (NA为阿伏伽德罗常数的值)
D.NiMH电池中不能用KOH溶液作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
 有 CH3CH2OH、CH3CH2Br、NH4Cl溶液四种无色液体,只用一种试剂就能把它们鉴别开,这种试剂是( )
有 CH3CH2OH、CH3CH2Br、NH4Cl溶液四种无色液体,只用一种试剂就能把它们鉴别开,这种试剂是( )
A.溴水 B.NaOH溶液
C.Na2SO4溶液 D.Br2的CCl4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同
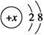 B.某金属阳离子的结构示意图为: 其与Cl-形成的强电解质都是离子化合物
B.某金属阳离子的结构示意图为: 其与Cl-形成的强电解质都是离子化合物
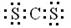 C.二硫化碳是直线形非极性分子,其电子式为:
C.二硫化碳是直线形非极性分子,其电子式为:
D.中子数为18的氯原子可表示为18Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
食品安全是现今百姓生活中热议问题之一,瘦肉精学名盐酸克伦特罗,白色或类白色
的结晶粉末,无臭、味苦,熔点161℃,溶于水、乙醇,微溶于丙酮,不溶于乙醚。其结
构简式如下图。有关瘦肉精的说法不正确 ( )
 A.化学式为C12H18ON2C12
A.化学式为C12H18ON2C12
B.遇FeCl3溶液发生显色反应
C.属于芳香族化合物
D.可以发生取代、加成、酯化、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.下图是某煤化工产业链的一部分,试运用所学知识,解决下列问题:
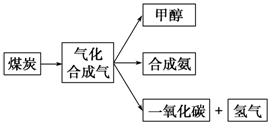
(1)已知该产业链中某反应的平衡常数表达式为
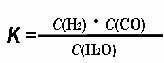 ,它所对应反应的化学方程式是 。
,它所对应反应的化学方程式是 。
(2)合成甲醇的主要反应是2H2(g)+CO(g)  CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率v(H2)=________。
②比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
③反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡______(填“逆向”、“正向”或“不”)移动,平衡常数K____________(填“增大”、“减小”或“不变”)。
(3)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:
N2(g)+O2(g)===2NO(g) ΔH=+180.8 kJ·mol-1,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是________________________________
(填字母序号)。
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2 000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
A.常温下,大气固氮和工业固氮都能非常容易进行
B.常温下,大气固氮与工业固氮完成程度相差不大
C.工业固氮时温度越低,氮气与氧气反应越完全
D.K越大说明合成氨反应的速率越大
Ⅱ. 科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导正极生成的O2-。
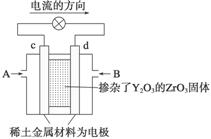
(1)c电极的名称为________。
(2)d电极上的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
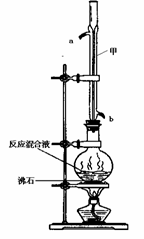 苯甲酸甲酯是一种重要的工业原料,某化学小组采用如右图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯。有关物质的物理性质见下表所示:
苯甲酸甲酯是一种重要的工业原料,某化学小组采用如右图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯。有关物质的物理性质见下表所示:
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入0.1mol苯甲酸和0.4mol 甲醇,再小心加入 3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)甲装置的作用是: ;冷却水从 (填“a”或“b”)口进入。
(2)化学小组在实验中用过量的反应物甲醇,其理由是 。
Ⅱ.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制

(1)试剂1可以是 (填编号),作用是 。
A.稀硫酸 B.碳酸钠溶液 C. 乙醇
(2)操作2中,收集产品时,控制的温度应在 ℃左右。
(3)实验制得的苯甲酸甲酯精品质量为10g,则苯甲酸的转化率为 (结果保留三位有效数字)。
(4)本实验制得的苯甲酸甲酯的产量低于理论产量,可能的原因是 (填编号)。
A.蒸馏时从100℃开始收集产品 B.甲醇用量多了 C.制备粗品时苯甲酸被蒸出
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制硫酸的第二步反应:

 △H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是( )
△H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是( )
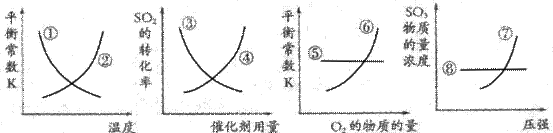
A. ①⑥⑧ B. ①⑤⑦ C. ②③④ D. ③⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com