
【题目】有机物G是一种香料,可采用丙烯和甲苯为主要原料按下列路线合成:
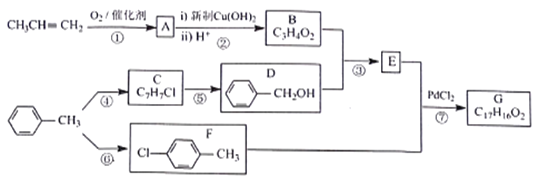
已知:①A的相对分子质量为56,其中氧的质量分数为28.6%
回答下列问题:
(1)A的分子式为___________,F的名称是__________
(2)B中含有的官能团名称为 __________________
(3)③的反应类型为_____________,反应⑤的试剂及条件为___________
(4)反应⑦的化学方程式为__________________
(5)X比D多1个CH2原子团,X的同分异构体中,能与FeCl3溶液发生显色反应的有______种,写出一种属于D的同系物且能发生消去反应的X的结构简式:______
【答案】C3H4O 4-氯甲苯或对氯甲苯 碳碳双键、羧基 酯化反应(取代反应) NaOH水溶液、加热  9
9 ![]() 或
或![]()
【解析】
已知A的相对分子质量为56,其中氧的质量分数为28.6%,A是丙烯氧化后的产物,则A中含有3个碳原子,1个氧原子,4个氢原子,分子式为C3H4O,不饱和度为2,由流程图可知A能与新制氢氧化铜反应生成B,说明A含有醛基,B含有羧基,则A的结构简式为
CH2=CHCHO,B的结构简式为CH2=CHCOOH,由B和D的结构简式可知,B和D发生酯化反应生成的E为![]() ,E和F生成G,G的结构简式为
,E和F生成G,G的结构简式为![]() ,由D的结构简式可推知C为
,由D的结构简式可推知C为![]() ,据此答题。
,据此答题。
(1)由上述分析可知A的分子式为C3H4O,根据F的结构简式可知F的名称为4-氯甲苯或对氯甲苯,故答案为:C3H4O;4-氯甲苯或对氯甲苯。
(2)由上述分析可知B的结构简式为CH2=CHCOOH,则B中含有的官能团的名称为碳碳双键、羧基,故答案为:碳碳双键;羧基。
(3)反应③是B和D发生酯化反应生成E为![]() ,由分析可知反应⑤是卤代烃的水解反应,需要的试剂为NaOH水溶液,条件为加热,故答案为:酯化反应(取代反应);NaOH水溶液、加热。
,由分析可知反应⑤是卤代烃的水解反应,需要的试剂为NaOH水溶液,条件为加热,故答案为:酯化反应(取代反应);NaOH水溶液、加热。
(4)反应⑦是E和F生成G,由E和F的结构简式可知其化学方程式为: ,
,
故答案为: 。
。
(5)D为![]() ,X比D多1个CH2原子团,则X的分子式为C8H10O,能与FeCl3溶液发生显色反应说明含有酚羟基,则可能的结构有9种:
,X比D多1个CH2原子团,则X的分子式为C8H10O,能与FeCl3溶液发生显色反应说明含有酚羟基,则可能的结构有9种:
 ,
,
而属于D的同系物,说明含有醇羟基,羟基不直接连在苯环上,且能发生消去反应,说明连有羟基碳原子的邻碳上有氢原子,则满足条件的X的结构简式为:![]() 或
或![]() ,故答案为:9;
,故答案为:9;![]() 或
或![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
A. 节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
C. 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
D. 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某化学兴趣小组探究化学能转变为电能的装置。

(1)当电极a为Zn、电极b为Fe、电解质溶液为稀硫酸时,SO42-向_____极(填a或b)移动,正极的电极反应式为:_____________
(2)若依据氧化还原反应:Cu+2Fe3+=Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的_______极,发生的电极反应式为:_______,电极a上发生的电极反应为______(填“氧化”或“还原”)反应。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入_____极(填a或b)。a极发生电极反应式为:________。当电路中通过2mol电子时,理论上消耗标况下氧气_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CH3COCH3(1) ![]() CH3COCH2COH(CH3)2(1)。取等量CH3COCH3分别在0℃和20℃下反应,测得其转化率(α)随时间(t)变化的关系曲线如下图所示。下列说法正确的是( )
CH3COCH2COH(CH3)2(1)。取等量CH3COCH3分别在0℃和20℃下反应,测得其转化率(α)随时间(t)变化的关系曲线如下图所示。下列说法正确的是( )
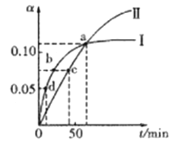
A. 化学反应速率的大小顺序为:d>b>c
B. 升高温度能提高反应物的平衡转化率
C. 在a点时,曲线Ⅰ和Ⅱ表示反应的化学平衡常数相等
D. 曲线Ⅱ表示20℃时的转化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010,下列有关说法中正确的是( )
A. 溶液的pH=4
B. 加蒸馏水稀释后,c(HA)/c(A-)减小
C. 向体积和pH均相等的HA溶液与盐酸中加入足量锌,盐酸中产生的气体多
D. 在NaA溶液中存在浓度关系:c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
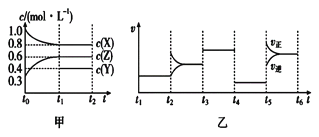
A. Y的起始物质的量为0.5mol
B. 该反应的化学方程式为2X(g)+Y(g)![]() 3Z(g) ΔH<0
3Z(g) ΔH<0
C. 若t0 =0,t1=10s,则t0~t1阶段的平均反应速率为v(Z)=0.03mol·L-1·s-1
D. 反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A~K均为中学化学中的常见物质,它们之间的转化关系如图所示,其中A、D为金属单质,反应过程中生成的水及其他部分产物已略去。
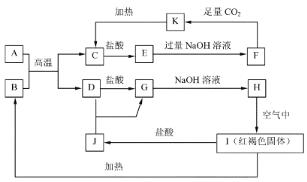
请回答以下问题:
(1)C是__,G是__。(填化学式)
(2)H生成I反应的化学方程式为__。
(3)向F中通入过量CO2生成K的离子方程式为__。
(4)E的溶液可以做净水剂,用离子方程式和必要的文字解释其净水原理:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质中均含有同一种元素M,它们之间有如图所示的转化关系。A为一种金属单质,其产量直接关系国民经济命脉。反应①②③均为化合反应,反应④为置换反应。下列有关说法错误的是
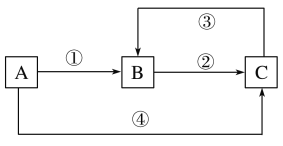
A. ①中所加试剂可能是氯气
B. ③中需要加具有氧化性的试剂
C. 元素M在②中发生的价态变化也能通过加碘化钾溶液实现
D. A与稀硝酸反应一定能实现元素M在①中发生的价态变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见金属单质A、B和气体甲、乙及C、D、E、F之间发生如下反应(图中有些反应所需的反应条件和部分产物没有全部标出)。
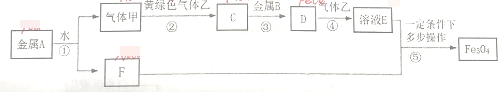
按要求回答下列问题:
(1)金属A元素在周期表中的位置为____;黄绿色气体乙的分子式为____;
(2)在①~⑤的反应中属于置换反应的有___;
(3)写出反应①的离子方程式____;
(4)写出反应④的离子方程式___;
(5)若33.6g的金属B完全反应,则在第④步反应中需消耗标准状况下__L的气体乙。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com