
��֪��
�� A��B��C��D�������ʾ���Ԫ��X���еĻ����ܺ���Ԫ��Y��Z��Ԫ��X��Y��Z��ԭ���������ε�����
�� X��A��B��C��D�ж���������������ϼۡ�
�������µ���A��ij�ֳ���һԪǿ����Һ��Ӧ���ɵõ�B��C��
�ܻ�����D���ȴ��ֽ⣬���Ƶ�Ԫ��Y�ĵ��ʡ�
(1)Ԫ��X�� ��Z�� ??����Ԫ��������գ���?
(2)д�����з�Ӧ�Ļ�ѧ����ʽ�� ��
(3)д�����з�Ӧ�Ļ�ѧ����ʽ�� ��
����4�֣�(1) Cl(����)��K(���)
(2)Cl2��2KOH��KCl��KClO��H2O (3)2KClO3 2KCl+3O2��
2KCl+3O2��
���������������1�������µ���A��ij�ֳ���һԪǿ����Һ��Ӧ���ɵõ�B��C����A��B��C�ж�����X��˵��A�м��з������绯��Ӧ���������������Һ�����绯��Ӧ������ѧ��ѧ����Ҫ��Cl2��Br2�ȣ�������D���ȴ��ֽ⣬���Ƶ�Ԫ��Y�ĵ��ʣ���֪ӦΪKClO3���ɴ˿�֪XΪO��YΪCl��ZΪK��AΪCl2��DΪKClO3��
��2��Cl2�ڼ�����Һ�з�������������ԭ��Ӧ������KCl��KClO������ʽΪCl2��2KOH��KCl��KClO��H2O��
��3��KClO3�ڴ��������¼��ȷֽ�����O2�����������غ㶨�ɿ�д����ѧ����ʽ��������ѧ����ʽ��2KClO3 2KCl+3O2����
2KCl+3O2����
���㣺���������ƶϵ��й��ж�
�������������е��Ѷȵ����⣬��Ҫ�ǿ���ѧ����Ԫ�ػ�����֪ʶ����Ϥ�˽�̶ȣ�ּ����������������û���֪ʶ���ʵ�����������������Ĺؼ�����ͻ�ƿڣ��ٽ�϶��������ʵ��˽⣬�²��һЩ����C12��KC1O3�ȣ�Ȼ��˳�ơ����ƺ������֤�����ȷ����ȫ���𰸣�����������ѧ���������������ͷ�ɢ˼ά������


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
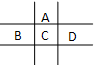
 ��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ��
��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���ش��������⣺
��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ��
��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1mol E���������������ã��ڱ�״�����ܲ���33.6L H2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ��
��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1mol E���������������ã��ڱ�״�����ܲ���33.6L H2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
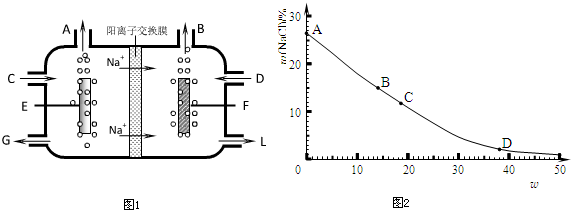
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com