
【题目】某工厂的工业废水中含有大量的![]() 和较多的
和较多的![]() 和
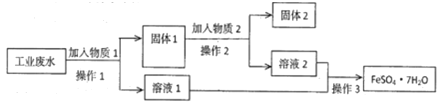
和![]() 为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
![]() 检验废水中的
检验废水中的![]() ,实验室中用酸性
,实验室中用酸性![]() 溶液检验,发生反应的离子方程式为______。
溶液检验,发生反应的离子方程式为______。
![]()
![]() 加入过量物质1后,发生反应的离子方程式为______。
加入过量物质1后,发生反应的离子方程式为______。
![]() 固体2是______,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入______。
固体2是______,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入______。
【答案】![]()
![]() 、
、![]() 铜
铜![]() 或
或![]() 铁粉
铁粉![]() 或
或![]()
【解析】
工业废水中含大量硫酸亚铁和较多的![]() 和
和![]() ,从该废水中回收硫酸亚铁和金属铜,先加过量铁,铁在金属活动顺序表中排在铜的前面,所以铁粉把铜置换出来,结合流程可知,操作1为过滤,过滤出Cu,Fe,滤液1是
,从该废水中回收硫酸亚铁和金属铜,先加过量铁,铁在金属活动顺序表中排在铜的前面,所以铁粉把铜置换出来,结合流程可知,操作1为过滤,过滤出Cu,Fe,滤液1是![]() ,Cu、Fe中加入
,Cu、Fe中加入![]() ,铁与硫酸反应,铜不反应,操作2为过滤,得到固体2为Cu,滤液中主要含
,铁与硫酸反应,铜不反应,操作2为过滤,得到固体2为Cu,滤液中主要含![]() ,操作3为蒸发、浓缩、结晶、过滤,可得到
,操作3为蒸发、浓缩、结晶、过滤,可得到![]() ,以此解答该题。
,以此解答该题。
![]() 亚铁离子与高锰酸钾发生氧化还原反应,反应的离子方程式为
亚铁离子与高锰酸钾发生氧化还原反应,反应的离子方程式为![]() ;
;
![]() 含有铁离子、铜离子,加入过量物质铁后,发生反应的离子方程式为
含有铁离子、铜离子,加入过量物质铁后,发生反应的离子方程式为![]() 、
、![]() ;
;
![]() 由以上分析可知固体2为铜
由以上分析可知固体2为铜![]() 或
或![]() ,硫酸亚铁具有还原性,可被氧化,可加入铁粉,防止被氧化, 故答案为:铜
,硫酸亚铁具有还原性,可被氧化,可加入铁粉,防止被氧化, 故答案为:铜![]() 或
或![]() ;铁粉
;铁粉![]() 或
或![]() 。
。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符合的是( )
A.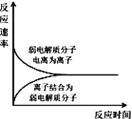 表示弱电解质在水中建立电离平衡的过程
表示弱电解质在水中建立电离平衡的过程
B.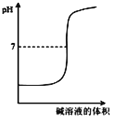 表示强碱滴定强酸的滴定曲线
表示强碱滴定强酸的滴定曲线
C.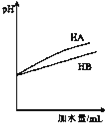 表示等体积等pH的弱酸HA和强酸HB加水稀释过程中的pH变化趋势
表示等体积等pH的弱酸HA和强酸HB加水稀释过程中的pH变化趋势
D.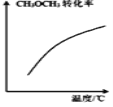 表示密闭容器中
表示密闭容器中![]() 达到平衡后,恒压升高温度过程中,
达到平衡后,恒压升高温度过程中,![]() 的转化率变化趋势
的转化率变化趋势
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是( )
A. Cu2+的价电子排布式为3d84s1
B. 所有氧原子都采取sp3杂化
C. 氧原子参与形成离子键、配位键和氢键三种化学键
D. 胆矾中的水在不同温度下会分步失去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求答下列有关问题。
Ⅰ.由乙烷和乙烯都能制得一氯乙烷。
(1) 由乙烷制一氯乙烷的化学方程式为____________,反应类型为______________。
(2)由乙烯制一氯乙烷的化学方程式为____________,反应类型为______________。
(3)以上两种方法中_________(填“(1) ”或“(2 ) ” )更适合用来制取一氯乙烷,原因是_________________。
Ⅱ.分别用一个化学方程式解释下列问题。
(4)甲烷与氯气的混合物在漫射光下—段时间,出现白雾:__________________。
(5)溴水中通入乙烯,溴水颜色退去:_________________________。
(6)工业上通过乙烯水化获得乙醇:______________________________。
Ⅲ.(7)下列关于苯的叙述正确的是__________(填序号)。
A.苯的分子式为C6H6,它不能使酸性KmnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.二甲苯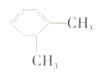 和
和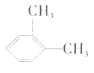 的结构不同,互为同分异构体
的结构不同,互为同分异构体
D.苯分子中的12个原子都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸中二氧化硫的催化氧化原理为:2SO2(g)+O2(g)![]() 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是

A. 在A、B、C三点时,V(正)=v(逆),在D点时V(正)>v(逆)
B. A、B、C三点的平衡常数一定不相同
C. 升高温度可以加快化学反应速率,有利于平衡向正反应方向移动
D. 一定温度下,保持容器体积不变,向平衡体系中通人稀有气体,压强增大,平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )

A. 溶液中一定不含CO32﹣,可能含有SO42-和NO3-
B. 溶液中n(NH4+)="0.2" mol
C. 溶液中的阳离子只有H+、Mg2+、Al3+
D. n(H+)︰n(Al3+)︰n(Mg2+)=1︰1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学欲在实验室中用乙醇制备1,2-二溴乙烷。
甲同学设计的实验装置如下图:
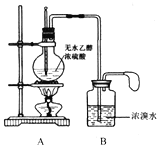
(1)请写出A和B中发生的主要反应的化学方程式
A:________________________________________。
B:________________________________________。
(2)乙同学查阅资料得知:
①此反应可能存在的主要副反应有:在浓硫酸的存在下,乙醇可发生如下反应生成乙醚, ![]()
②乙醚不与溴水反应
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
颜色、状态 | 无色液体 | 无色液体 | 无色液体 |
沸点/℃ | 78.5 | 132 | 34.6 |
若最终产物中混有少量乙醚,可用__________的方法除去。
(3)丙同学观察到:在实验后期A中液体变黑,认为应该在装置A和B之间加入装置__________(填序号),此装置的作用是____________________。
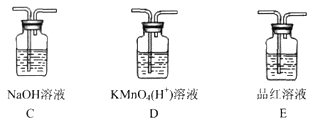
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在密闭容器中进行下列反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
(1)增加C(s),平衡___。
(2)减小密闭容器容积,保持温度不变,则平衡___。
(3)通入N2,保持密闭容器容积和温度不变,则平衡__。
(4)保持密闭容器容积不变,升高温度,则平衡__。
Ⅱ.在一密闭容器中发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。
2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。
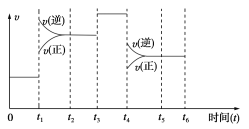
下列时间段中,氨的百分含量最高的是(_____)
A.0~t1 B.t2~t3
C.t3~t4 D.t4~t5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com