
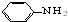 +CH3COOH
+CH3COOH| △ |
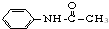 +H2O
+H2O| 名称 | 式量 | 性状 | 密度/g/cm3 | 沸点/℃ | 溶解度 | |
| 苯 胺 | 93 | 无色油状液体, 具有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
| 乙 酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水, 溶于热水 | 易溶于乙醇、乙醚 |
 注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离

科目:高中化学 来源: 题型:
| A、在硅酸钠溶液中滴加酚酞 |
| B、碳酸钠溶液中滴加酚酞 |
| C、硫酸铁溶液中滴加硫氰化钾溶液 |
| D、碳酸氢钠溶液中滴加稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A为非电解质 |
| B、A是强电解质 |
| C、A是分子晶体 |
| D、A为弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | ① | ② | ③ | ④ |
| 装置 |  |  | 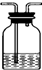 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:
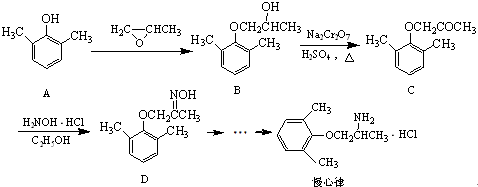
 ).写出以邻甲基苯酚(
).写出以邻甲基苯酚(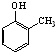 )和乙醇为原料制备
)和乙醇为原料制备 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
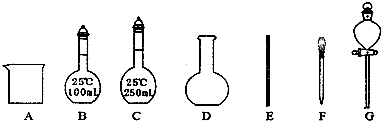
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com