
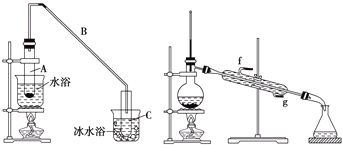
【题目】化学小组采用类似制乙酸乙酯的装置(如下图),用环己醇制备环己烯。
已知: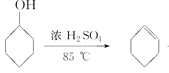 +H2O
+H2O
密度 | 熔点 | 沸点 | 溶解性 | |
环己醇 |
| 25 | 161 | 能溶于水 |
环己烯 |
|
| 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片(防止暴沸),缓慢加热至反应完全,在试管C内得到环己烯粗品。
导管B除了导气外还具有的作用是______。
②试管C置于冰水浴中的目的是______。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等![]() 加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用______(填入编号)洗涤。
加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用______(填入编号)洗涤。
A.KMnO4溶液![]() 稀H2SO4 C.Na2CO3溶液
稀H2SO4 C.Na2CO3溶液
②再将环己烯按上图装置蒸馏,冷却水从______口进入![]() 填“g”或“f”),蒸馏时要加入生石灰,其目的是______。
填“g”或“f”),蒸馏时要加入生石灰,其目的是______。
③收集产品时,控制的温应在______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是_____。
A.蒸馏时从![]() 开始收集产品
开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是______。
A.分别加入酸性高锰酸钾溶液
B.分别加入用金属钠
C.分别测定沸点
【答案】冷凝 防止环己烯的挥发 上 C g 除去水分 83℃ C BC
【解析】
(1)①由于生成的环己烯的沸点为83℃,要得到液态环己烯,导管B除了导气外还具有冷凝作用,便于环己烯冷凝;
②冰水浴的目的是降低环己烯蒸气的温度,使其液化;
(2)①环己烯不溶于氯化钠溶液,且密度比水小,分层后环己烯在上层,由于分液后环己烯粗品中还含有环己醇,提纯产物时用c(Na2CO3溶液)洗涤;
②为了增加冷凝效果,冷却水从下口(g)进入;生石灰能与水反应生成氢氧化钙,利于环己烯的提纯;
③根据表中数据可知,馏分环己烯的沸点为83℃;粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量;
(3)根据混合物没有固定的沸点,而纯净物有固定的沸点,通过测定环己烯粗品和环己烯精品的沸点,可判断产品的纯度。
(1)①由于生成的环己烯的沸点为![]() ,要得到液态环己烯,导管B除了导气作用外,还具有冷凝作用,便于环己烯冷凝;
,要得到液态环己烯,导管B除了导气作用外,还具有冷凝作用,便于环己烯冷凝;
②冰水浴的目的是降低环己烯蒸气的温度,使其液化;
(2)①环己烯是烃类,属于有机化合物,在常温下呈液态,不溶于氯化钠溶液,且密度比水小,振荡、静置、分层后,环己烯在上层。由于浓硫酸可能被还原为二氧化硫气体,环己醇易挥发,故分液后环己烯粗品中还含有少量环己醇,还可能溶解一定量的二氧化硫等酸性气体,联想制备乙酸乙酯提纯产物时用饱和碳酸钠溶液洗涤可除去酸性气体并溶解环己醇,除去杂质。稀硫酸不能除去酸性气体,高锰酸钾溶液会将环己烯氧化,因此合理选项是C;
②为了增加冷凝效果,蒸馏装置要有冷凝管,冷却水从下口(g)进入,生石灰能与水反应生成氢氧化钙,除去了残留的水,然后蒸馏,就可得到纯净的环己烯;
③根据表中数据可知,馏分环己烯的沸点为83℃,因此收集产品应控制温度在83℃左右,若粗产品中混有环己醇,会导致环己醇的转化率减小,故环己烯精品质量低于理论产量,故合理选项是C;
(3)区别粗品与精品的方法是向待检验物质中加入金属钠,观察是否有气体产生,若无气体,则物质是精品,否则就是粗品,也可以根据物质的性质,混合物由于含有多种成分,没有固定的沸点,而纯净物只有一种成分组成,有固定的沸点,通过测定环己烯粗品和环己烯精品的沸点,可判断产品的纯度,因此合理选项是BC。


科目:高中化学 来源: 题型:
【题目】8月12日晚11时20分左右,天津港国际物流中心区域内瑞海公司所属危险品仓库发生的爆炸,造成了严重的人员伤亡,据瑞海国际官网信息,该公司仓储含有以下种类物质:压缩气体天然气、易燃液体乙酸乙酯、遇湿易燃物品电石、腐蚀品硫化碱等。
回答下列问题:
(1)天然气的主要成分为______(填分子式),试写出它的两种重要用途_________________;
(2)电石的主要成分为CaC2,遇水会剧烈反应生成可燃性气体乙炔(C2H2),CaC2属于_______化合物(填“离子”或“共价”);电石引发的火灾应该可用__扑灭。
A.泡沫灭火器 B.消防车喷水 C.沙土
(3)易燃液体乙酸乙酯是我们比较熟悉的一种化合物,新酿制的酒里含有少量乙醛,所以入口较为生、涩,请用化学反应方程式来表示这一过程_____;
(4)硫化碱其实就是我们常见的硫化钠,触及皮肤和毛发时会造成灼伤。①其水溶液呈强碱性,故俗称硫化碱.原因是(用离子方程式表示)________________;②其水溶液在空气中会缓慢地氧化成硫代硫酸钠(Na2S2O3),写出该反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+ B2= 2AB的能量变化如图所示,则下列说法正确的是( )

A. 该反应是吸热反应
B. 断裂1 mol A—A键和1 mol B—B键能放出x kJ的能量
C. 断裂2 mol A—B键需要吸收y kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键类型的叙述正确的是( )
A.全部由非金属构成的化合物中肯定不存在离子键
B.所有物质中都存在化学键
C.已知乙炔的结构式为H—C≡C—H,则乙炔中存在2个σ键(C—H)和3个π键(C≡C)
D.乙烷分子中只存在σ键,不存在π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,通入的气体物质只作为氧化剂的是
A.二氧化硫通入溴水溶液中B.氯气通入氯化亚铁溶液中
C.一氧化碳气体通入灼热的CuO中D.二氧化氮通入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )

A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
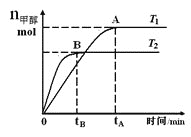
A. 平衡常数K=![]()
B. 该反应在T1时的平衡常数比T2时的小
C. CO合成甲醇的反应为吸热反应
D. 处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______,基态铜原子中,核外电子占据最高能层的符号是______,占据该最高能层的电子数为__________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________(填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为_____________。硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是异硫氰酸(H-N=C=S)。理论上前者沸点低于后者,其原因是____________________________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________。
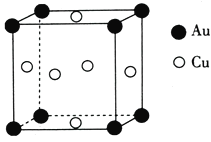
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____![]() 用含a、NA的代数式表示)gcm-3。
用含a、NA的代数式表示)gcm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com