
【题目】下列物质不能发生水解的是
A. 葡萄糖 B. 油脂 C. 淀粉 D. 蛋白质
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用.
(1)已知:①CH4(g)+H2O(g)CO(g)+3H2(g)△H1=+206.1kJmol﹣1
②2H2(g)+CO(g)CH3OH(l)△H2=﹣128.3kJmol﹣1
③2H2(g)+O2(g)2H2O (g)△H3=﹣483.6kJmol﹣1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为 .
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa).
实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/molL﹣1 | H2O初始浓度/molL﹣1 |
1 | 400 | p | 3.0 | 7.0 |
2 | t | 101 | 3.0 | 7.0 |
3 | 400 | 101 | 3.0 | 7.0 |
①实验2和实验3相比,其平衡常数关系是K2K3(填“>”、“<”或“=”).
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为 .
(3)科学家提出由CO2制 取 C的太阳能工艺如图1所示.
①“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则Fe xOy的化学式为 .
②“热分解系统”中每分解l mol Fe xOy , 转移电子的物质的量为 . 
(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值.若某溶液中溶质的浓度为1×10﹣3molL﹣1 , 则该溶液中溶质的pC=﹣lg(1×10﹣3)=3.如图2为25℃时H2CO3溶液的pC﹣pH图.请回答下列问题 (若离子浓度小于10﹣5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3﹣、CO32﹣(填“能”或“不能”)大量共存.
②求H2CO3一级电离平衡常数的数值Ka1= .
③人体血液里主要通过碳酸氢盐缓冲体系 ![]() 可以抵消少量酸或碱,维持pH=7.4.当过量的酸进入血液中时,血液缓冲体系中的
可以抵消少量酸或碱,维持pH=7.4.当过量的酸进入血液中时,血液缓冲体系中的 ![]() 最终将 .
最终将 .
A.变大B.变小C.基本不变D.无法判断.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨气的制备和性质实验装置的说法中正确的是( )
A.用图1装置制取NH3
B.用图2装置实验室制备NaAlO2溶液
C.用图3装置可以完成“喷泉”实验
D.用图4装置测量反应产生氨气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 水玻璃、玻璃、水泥、陶瓷均为混合物
B. CO2、SiO2、CO均为酸性氧化物
C. SiC的俗名叫金刚砂,硬度很大
D. 实验室熔融烧碱时,不能使用石英坩埚,可以使用铁坩埚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)用铜、银与硝酸银设计一个原电池,此电池的负极是 , 负极的电极反应式是 .
(2)如图为氢氧燃料碱性电池,电极材料为疏松多孔石墨棒. 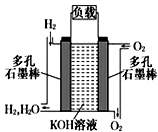
根据所学知识试回答下列问题:
①写出氢氧燃料电池工作时正极电极反应方程式: .
②如果该氢氧燃料电池每转移1mol电子,消耗标准状况下氧气的体积为 .
③阳离子向极移动(填写正或负),反应一段时间后整个溶液的碱性(填增强,减弱或者不变).
④若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质之间的反应没有明显反应现象的是( )
A. 将CO2通入硝酸钡中
B. 用玻璃棒分别蘸取浓盐酸和浓氨水并相互靠近
C. 硅酸钠溶液中通入二氧化碳
D. 将氯化氢气体通入滴有酚酞的烧碱溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )
①2:7 ②5:4 ③4:5 ④7:2.
A.①②
B.③④
C.②④
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl﹣、SO42﹣ , 现分别取100mL的两份溶液进行如下实验.
①第一份加过量NaOH溶液后加热,收集到0.03mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2 , 生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到23.3g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
A.由①可知原溶液存在离子为NH4+ , 其浓度为0.03mol/L
B.原溶液肯定没有Fe3+、Mg2+ , 一定含有Na+
C.n(NH4+):n(Al3+):n(SO42﹣)=3:1:10
D.原溶液一定存在Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物.
(1)请写出下列元素的元素符号:Z , W;请写出Y2O2的电子式: .
(2)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式):
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应,请写出实验室制备该气体的化学反应方程式;检验该气体是否收集满的操作方法
(4)Q是和Y同一主族的原子序数最大的元素,下列关于Q的说法正确的有 A.熔点较低
B.不与水反应
C.其最高价氧化物对应水化物为碱性
D.可以电解其熔融态的氯化物制取
E.碳酸盐受热易分解为氧化物和二氧化碳.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com