
【题目】西他沙星是一种广谱喹诺酮类抗菌药,可用于治疗严重的感染性疾病。一种合成西他沙星中间体![]() 的合成路线如下图所示:
的合成路线如下图所示:
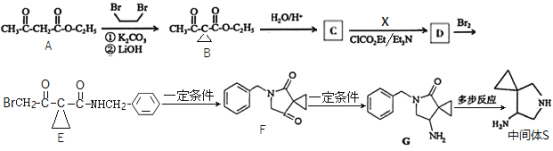
回答下列问题:
(1)![]() 的化学名称是__________。
的化学名称是__________。
(2)![]() 的结构简式为__________,
的结构简式为__________,![]() 生成
生成![]() 的反应类型是__________。
的反应类型是__________。
(3)![]() 生成
生成![]() 的化学方程式为_________________________________。
的化学方程式为_________________________________。
(4)X的同分异构体中,与X含有相同的官能团,且含苯环的有__________种(不考虑立体异构,![]() 除外);其中,核磁共振氢谱峰面积比为3:2:2:2的物质结构简式为__________(写化学式)。
除外);其中,核磁共振氢谱峰面积比为3:2:2:2的物质结构简式为__________(写化学式)。
(5)写出![]() 为原料制备
为原料制备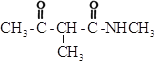 的合成路线:__________(其他试剂任选)。
的合成路线:__________(其他试剂任选)。
【答案】1,2-二溴乙烷 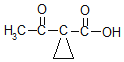 取代反应
取代反应 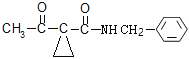 +Br2→
+Br2→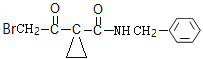 +HBr 3
+HBr 3 ![]()
![]()

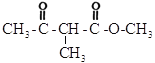
![]()
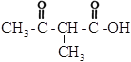
![]()
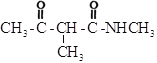
【解析】
A(![]() )与BrCH2CH2Br在①碳酸钠,②LiOH作用下反应生成B(
)与BrCH2CH2Br在①碳酸钠,②LiOH作用下反应生成B(![]() ),B在酸性条件下水解生成C,C为
),B在酸性条件下水解生成C,C为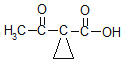 ;由E的结构简式(
;由E的结构简式(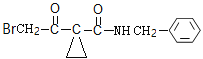 )和D→E的条件可知,D为
)和D→E的条件可知,D为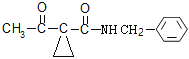 ,结合流程图中官能团的性质和变化分析解答。
,结合流程图中官能团的性质和变化分析解答。
(1) ![]() 的名称是1,2-二溴乙烷,故答案为:1,2-二溴乙烷;
的名称是1,2-二溴乙烷,故答案为:1,2-二溴乙烷;
(2)根据上述分析可知,C为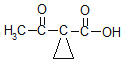 。对比
。对比![]() (
(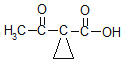 )、
)、![]() (
(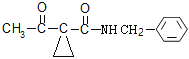 )的结构简式可知
)的结构简式可知![]() 生成
生成![]() 是形成肽键的过程,属于取代反应,故答案为:
是形成肽键的过程,属于取代反应,故答案为: ;取代反应;
;取代反应;
(3)![]() (
(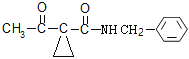 )生成
)生成![]() (
(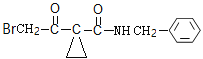 )是D中甲基上的氢原子被溴原子取代的过程,反应的化学方程式为
)是D中甲基上的氢原子被溴原子取代的过程,反应的化学方程式为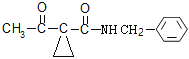 +Br2→
+Br2→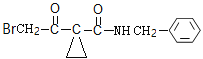 +HBr,故答案为:
+HBr,故答案为: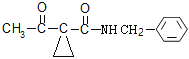 +Br2→
+Br2→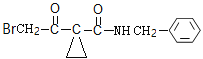 +HBr;
+HBr;
(4)X为![]() ,含氨基官能团,与甲基在苯环上的位置有邻、间、对3种;其中,核磁共振氬谱峰面积为3:2:2:2的物质为
,含氨基官能团,与甲基在苯环上的位置有邻、间、对3种;其中,核磁共振氬谱峰面积为3:2:2:2的物质为![]() ,故答案为:3;
,故答案为:3;![]() ;
;
(5)由已知合成路线知![]() 与
与![]() 发生取代反应生成
发生取代反应生成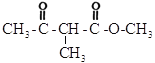 ,然后在酸性条件下水解生成
,然后在酸性条件下水解生成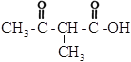 ,该物质的羧基与
,该物质的羧基与![]() 反应生成目标物质,故合成路线为:
反应生成目标物质,故合成路线为:![]()

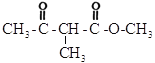
![]()
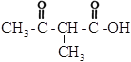
![]()
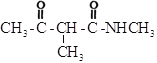 ,故答案为:
,故答案为:![]()

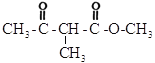
![]()
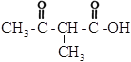
![]()
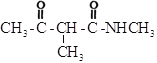 。
。


科目:高中化学 来源: 题型:
【题目】研究小组发现一种化合物在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4min~8min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是
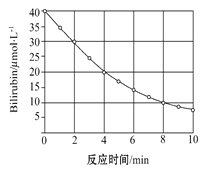
A. 2.5μmol·L-1·min-1和2.0μmol·L-1
B. 2.5μmol·L-1·min-1和2.5μmol·L-1
C. 3.0μmol·L-1·min-1和3.0μmol·L-1
D. 3.0μmol·L-1·min-1和2.5μmol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型氟离子电池的电解质为![]() 和
和![]() ,
,![]() 可嵌入这两种盐的晶体中,该电池工作时放电的示意图如图所示,下列判断正确的是( )
可嵌入这两种盐的晶体中,该电池工作时放电的示意图如图所示,下列判断正确的是( )
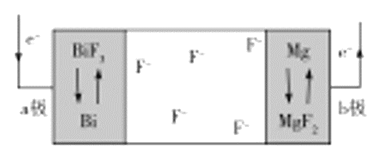
A.放电时,![]() 极为该电池的正极
极为该电池的正极
B.充电时,![]() 移向
移向![]() 极
极
C.充电时,阳极的电极反应式为![]()
D.电池总反应为![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是被广泛应用的金属之一,铜器件在空气中久置会生成铜锈:
是被广泛应用的金属之一,铜器件在空气中久置会生成铜锈:![]() 。回答下列问题:
。回答下列问题:
(1)![]() 元素在元素周期表中的位置为________,基态
元素在元素周期表中的位置为________,基态![]() 原子的核外电子排布式为________,基态
原子的核外电子排布式为________,基态![]() 有________个未成对电子。
有________个未成对电子。
(2)参与生成铜锈的物质![]() 中
中![]() 原子的杂化方式为________,
原子的杂化方式为________,![]() 分子的空间构型是________。
分子的空间构型是________。
(3)![]() 的晶体类型是________,
的晶体类型是________,![]() 含________
含________![]() σ键。
σ键。
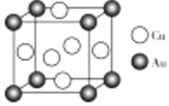
(4)![]() 、
、![]() 可形成金属互化物,其晶胞结构如图所示,若该
可形成金属互化物,其晶胞结构如图所示,若该![]() 、
、![]() 金属互化物的密度为
金属互化物的密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]() ,则晶胞边长
,则晶胞边长![]() =________nm;
=________nm;
(5)金属铜单独与氨水或过氧化氢均不能反应,但可与过氧化氢和过量氨水的混合溶液反应生成一种配位化合物,其反应的化学方程式可表示为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示。请回答下列问题:
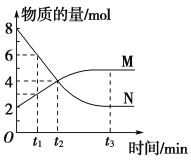
(1)该反应的化学方程式为___________。
(2)在t2时刻存在的等量关系是_____________,此时反应是否达到化学平衡状态?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的用途利用了其还原性的是( )
A. 用葡萄糖制镜子或保温瓶胆
B. 用硫粉覆盖洒落在桌上的Hg
C. 用![]() 溶液制备木材防火剂
溶液制备木材防火剂
D. 用![]() 作为高效水处理剂
作为高效水处理剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗硅中含有铁和锡(Sn)等杂质,粗硅与氯气反应可生成SiCl4,SiCl4经提纯后用氢气还原可得高纯硅。实验室用下列装置模拟制备SiCl4。已知:SiCl4的熔点是-70℃,沸点是57.6℃,易与水反应;Sn Cl4的熔点是-33℃,沸点是114℃
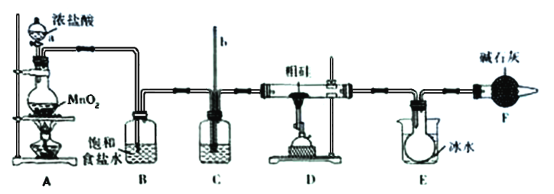
回答下列问题:
(1)仪器a的名称是_______;装置A烧瓶中发生反应的离子方程式是____________。
(2)装置C中盛放的试剂是_____________,作用是___________________;玻璃管b的作用是_______________________。
(3)装置E的烧杯中盛放冰水的目的是______________________。
(4)装置F中碱石灰的作用是____________________________。
(5)装置E烧瓶中得到的SiCl4中溶有少量的杂质FeCl3和SiCl4,可以通过___________方法提纯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种埋在地下的矿物X(仅含四种元素),挖出后在空气中容易发黄,现探究其组成和性质,设计完成如图实验:
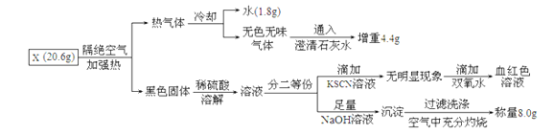
请回答:
(1)X的化学式____。
(2)X隔绝空气加热的化学反应方程式为:___。
(3)用化学方程式表示在空气中变黄的原因____。
(4)写出检验溶液A中存在的金属阳离子的实验方法:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com