
| 1800g |
| 18g/mol |
| 1800g |
| 18g/mol |


科目:高中化学 来源: 题型:
| A、甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B、澄清透明的溶液中:NH4+、Fe3+、SO42-、MnO4- |
| C、含大量Al3+的溶液中:AlO2-、Na+、NO3-、Ca2+ |
| D、含大量OH-的溶液中:HCO3-、Cl-、F-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
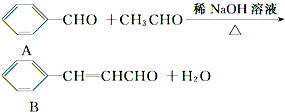
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 点燃 |
| 乙烷 | 丙烷 | 丁烷 | |
| 熔点/℃ | -183.8 | -189.7 | -138.4 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
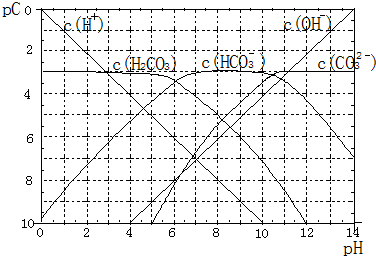
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
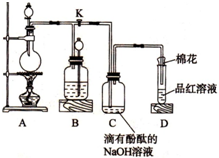 为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验,请回答:
为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com