
| ||
| ||



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢·Ö×ÓŹżĪŖNAµÄCO”¢C2H4»ģŗĻĘųĢåĢå»żŌ¼ĪŖ22.4L£¬ÖŹĮæĪŖ28g |
| B”¢³£ĪĀĻĀ£¬1 L 0.1 mol?L-1µÄNH4NO3ČÜŅŗÖŠNH4+ŗĶNO3-×ÜŹżĪŖ0.2 NA |
| C”¢±ź×¼×“æöĻĀ£¬4.48LÖŲĖ®£ØD2O£©ŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ2 NA |
| D”¢1mol¼×»ł£Ø-CH3£©Ėłŗ¬µē×ÓŹżĪŖ9NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
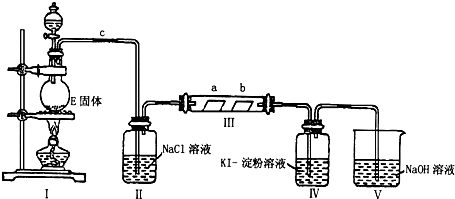
 ijĶ¬Ń§ĪŖĮĖ¼ģŃé¼ŅÖŠµÄŅ»Ęæ²¹ĢśŅ©£Ø³É·ÖĪŖFeS04£©ŹĒ·ń±äÖŹ£¬Éč¼ĘĮĖČēĻĀŹµŃé£ŗ½«Ņ©Ę¬³żČ„ĢĒŅĀŃŠĻøŗó£¬Čܽā¹żĀĖ£¬Č”ĀĖŅŗ·Ö±š¼ÓČėĮ½Ö§ŹŌ¹ÜÖŠ£¬ŌŁ½ųŠŠČēĻĀĶ¼ĖłŹ¾²Ł×÷£®
ijĶ¬Ń§ĪŖĮĖ¼ģŃé¼ŅÖŠµÄŅ»Ęæ²¹ĢśŅ©£Ø³É·ÖĪŖFeS04£©ŹĒ·ń±äÖŹ£¬Éč¼ĘĮĖČēĻĀŹµŃé£ŗ½«Ņ©Ę¬³żČ„ĢĒŅĀŃŠĻøŗó£¬Čܽā¹żĀĖ£¬Č”ĀĖŅŗ·Ö±š¼ÓČėĮ½Ö§ŹŌ¹ÜÖŠ£¬ŌŁ½ųŠŠČēĻĀĶ¼ĖłŹ¾²Ł×÷£® | ĻÖĻó | ½įĀŪ |
| ¢ŁÖŠĖįŠŌKMnO4ČÜŅŗĶŹÉ« ¢ŚÖŠKSCNČÜŅŗ²»±äÉ« | |
| ¢ŁÖŠĖįŠŌKMnO4ČÜŅŗ²»ĶŹÉ« ¢ŚÖŠKSCNČÜŅŗ±äŗģ | |
| ¢ŁÖŠĖįŠŌKMnO4ČÜŅŗĶŹÉ« ¢ŚÖŠKSCNČÜŅŗ±äŗģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
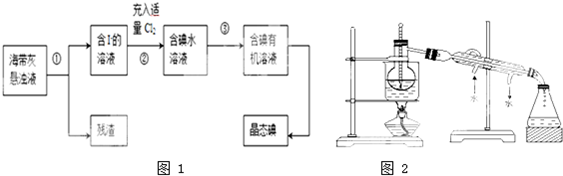
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ČÜÖŹ | ¼ÓČėŹŌ¼Į | Ąė×Ó·½³ĢŹ½ |
| Cu2+ | ||
| SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢·“Ó¦ŗóČÜŅŗÖŠ²»“ęŌŚČĪŗĪ³Įµķ£¬ĖłŅŌ·“Ó¦Ē°ŗóCu2+µÄÅØ¶Č²»±ä |
| B”¢³ĮµķČܽāŗ󣬽«Éś³ÉÉīĄ¶É«µÄÅäĄė×Ó[Cu£ØNH3£©4]2+ |
| C”¢Ļņ·“Ó¦ŗóµÄČÜŅŗ¼ÓČėŅŅ“¼£¬ČÜŅŗ½«»įƻӊ·¢ÉśČĪŗĪ±ä»Æ£¬Ņņ[Cu£ØNH3£©4]2+²»»įÓėŅŅ“¼·¢Éś·“Ó¦ |
| D”¢ŌŚ[Cu£ØNH3£©4]2+Ąė×ÓÖŠ£¬Cu2+øų³ö¹Ā¶Ōµē×Ó£¬NH3Ģį¹©æÕ¹ģµĄ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com