
| C% | H% | O% |
| 40.00% | 6.67% | 53.33% |
| 90×40.00% |
| 12 |
| 90×6.67% |
| 1 |
| 90×53.33% |
| 16 |


科目:高中化学 来源: 题型:
| A、吸热反应一定不能自发进行 |
| B、△H大于零的反应是放热反应 |
| C、已知S(单斜,s)=S(正交,s)△H<0,则单斜硫比正交硫稳定 |
| D、应用盖斯定律,可计算某些难以直接测量的反应的反应热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
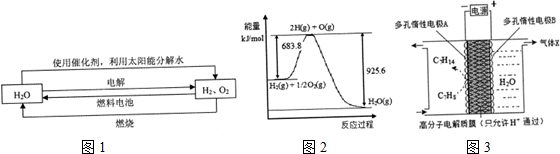
| ||
| ||
| 催化剂 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖和淀粉均属于高分子化合物 |
| B、鸡蛋清中加入 CuSO4 溶液会产生盐析 |
| C、14C可用于文物年代的鉴定,14C与14N互为同位素 |
| D、自由移动离子数目多的电解质溶液导电能力不一定强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
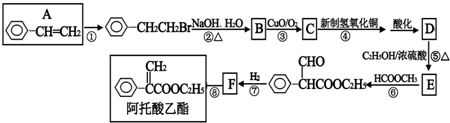
查看答案和解析>>
科目:高中化学 来源: 题型:
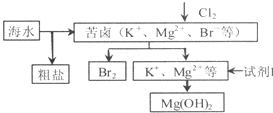 海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、从苦卤中提取Br2的离子方程式为2Br-+Cl2═2C1-十Br2 |
| C、试剂1可以选用Ca(OH)2 |
| D、工业上,电解熔融Mg(OH)2冶炼金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
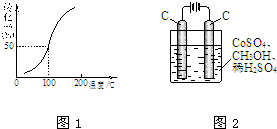 甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.
甲醇可作电池的原料,也会造成环境污染.请根据有关反应回答问题.| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
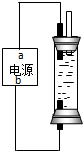 NaClO具有强氧化性,其溶液可用于游泳池及环境消毒.
NaClO具有强氧化性,其溶液可用于游泳池及环境消毒.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下溶解度:Na2CO3<NaHCO3 |
| B、热稳定性:Na2CO3<NaHCO3 |
| C、与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3 |
| D、与澄清石灰水反应,均有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com